Неоднородность - поверхность - адсорбент
Cтраница 2
Тэйлор выдвинул общую теорию адсорбции, согласно которой: а) для хемосорбции необходима энергия активации Е б) скорость хемосорбции зависит в первую очередь от Е, а также от температуры, давления газа, природы и неоднородности поверхности адсорбента. [16]
Вероятно, закрепление молекул хлорофилла на гидрофильной поверхности аэросила способствует образованию агрегатов пигмента определенной конфигурации. Агрегации хлорофилла способствует неоднородность поверхности адсорбента. [17]
Рассмотрено влияние качества поверхности адсорбента на форму хроматографиче-ской кривой. Показано, что неоднородность поверхности адсорбента является причиной несимметричности пиков. [18]
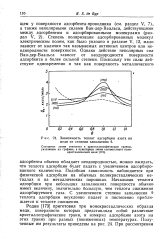 |
Зависимость теплот адсорбции азота на меди от степени заполнения 6. [19] |
Степень поляризации адсорбированных молекул электрическим полем, как было указано в разделе V, 12, мало зависит от наличия так называемых активных центров или неоднородности поверхности. Однако действие неполярных сил Ван-дер - Ваальса зависит от неоднородности поверхности адсорбента в более сильной степени. [20]
Если равновесная функция с увеличением 0 падает, то, по мнению Грэма, это свидетельствует о неоднородности поверхности адсорбента. Функция 9 / ( 1 - 6) может падать также при образовании на поверхности адсорбента энергетически неравноценных адсорбционных комплексов. [21]
Одной из задач молекулярной теории адсорбции является вычисление физико-химических характеристик ( констант адсорбционного равновесия, теплот и энтропии адсорбции, теплоемкости адсорбата) на основании свойств молекулы адсорбата и свойств адсорбента. Отклонения от предельного закона Генри связаны либо с притя жением адсорбат-адсорбат, либо с отталкиванием адсорбированных молекул друг от друга или с неоднородностью поверхности адсорбента. Влияние этих факторов пока не охарактеризовано количественно с помощью молекулярной теории. [22]
Одной из задач молекулярной теории адсорбции является вычисление физико-химических характеристик ( констант адсорбционного равновесия, теплот и энтропии адсорбции, теплоемкости адсорбата) на основании свойств молекулы адсорбата и свойств адсорбента. Отклонения от предельного закона Генри связаны либо с притя жением адсорбат-адсорбат, либо с отталкиванием адсорбированных моле кул друг от друга или с неоднородностью поверхности адсорбента. Влияние этих факторов пока не охарактеризовано количественно с помощью молекулярной теории. Поэтому представляют теоретический интерес и практическую ценность попытки расчета этих термодинамических функций с помощью приближенных уравнений адсорбционного равновесия [3-12], содержащих константы равновесия для различных вкладов взаимодействий в адсорбционных системах, в частности, для взаимодействия адсорбат - адсорбат. [23]
Развил ( 1925 - 1930) эти представления в теорию неоднородной поверхности, подкрепив ее экспериментально. Сформулировал ( 1931) общую теорию адсорбции, согласно которой: а) для хемо-сорбции необходима энергия активации Е; б) скорость хемосорбции зависит в первую очередь от Е, а также от температуры, давления газа, природы и неоднородности поверхности адсорбента. В дальнейшем эти положения были под - j тверждены всей историей учения о катализе. [24]
Поверхность адсорбентов обычно неоднородна. Это связано с особенностями их строения и получения. Неоднородность поверхности адсорбента очень усложняет математические зависимости, описывающие адсорбцию. Поэтому для получения простейших закономерностей обращаются к физической адсорбции идеального газа однородной поверхностью адсорбента. К адсорбентам с практически однородной поверхностью относится сажа, прокаленная при 3000 С. При адсорбции газа на саже образуется мономолекулярный адсорбционный слой, толщина которого определяется размерами молекул адсорбата и их ориентацией на поверхности адсорбента. [25]
Поверхность адсорбентов обычно неоднородна. Это связано с особенностями их строения и получения. Неоднородность поверхности адсорбента очень усложняет математические зависимости, описывающие адсорбцию. Поэтому для получения простейших закономерностей обращаются к физической адсорбции идеального газа однородной поверхностью адсорбента. К адсорбентам с практически однородной поверхностью относится сажа, прокаленная при 3000 С. При адсорбции газа на саже образуется мономолекулярный адсорбционный слой, толщина которого определяется размерами молекул адсорбата и их. [26]
Это явление аналогично экстракции, при которой также осуществляется распределительное равновесие. Преимущество распределительной хроматографии состоит, во-первых, в том, что жидких неподвижных фаз с различными свойствами намного больше, чем адсорбентов, и, во-вторых, в том, что в данном случае неподвижная фаза обладает гомогенной поверхностью, тогда как поверхность даже самых лучших адсорбентов содержит различные центры повышенной адсорбционной способности. Эта неоднородность поверхности адсорбента препятствует равномерной адсорбции или десорбции, снижая тем самым эффективность разделения колонки и, кроме того, делая почти невозможным разделение сильно адсорбируемых веществ. В случае жидкой неподвижной фазы, напротив, сильно адсорбируемые вещества могут быть разделены без труда. Так как имеются неподвижные фазы самой различной полярности, то в настоящее время хроматография может быть применена практически ко всем веществам, поскольку они в какой-то степени растворимы и летучи. Чтобы осуществить хроматографическое разделение пары веществ, достаточно иметь подходящую неподвижную фазу, в которой данные компоненты имели бы различную растворимость. [27]
 |
Изотерма адсорбции азота на различных пористых адсорбентах в координатах log /., а-2, по данным Гаркинса и Юра. [28] |
В действительности, в особенности на неоднородных поверхностях, свойства адсорбционных пленок точно не отвечают столь простому уравнению состояния. Кроме того, вряд ли можно согласиться с тем, что коэффициент пропорциональности К не зависит от природы поверхноститвердого тела, а независимое определение его для каждого типа адсорбентов представляет существенные трудности и пока еще не сделано. Отметим также, что неоднородность поверхности адсорбента и здесь может сильно исказить результаты определения s, так что метод Гаркинса и Юра также является лишь приближенным. [29]
Адсорбция даже таких простых газов, как водород, кислород, азот и окись углерода, на переходных металлах представляет собой весьма сложный процесс, поскольку в ходе адсорбции образуется несколько связанных форм. Слабо связанные состояния водорода и азота имеют, по-видимому, молекулярный характер и образуются в результате взаимодействия с переносом заряда, в то время как несколько прочно связанных состояний являются атомарными. Существование нескольких хемосорбционных состояний отчасти может быть следствием кристаллографической неоднородности поверхности поликристаллического адсорбента. Однако это не единственная причина, поскольку такая же сложная картина наблюдается при адсорбции на поверхностях. [30]
Страницы: 1 2 3