Неопентилгликоль
Cтраница 2
Комплексный эфир неопентилгликоля, дикарбоновой кислоты и одноатомного спирта по своей структуре относится к комплекскыы эфирам 2-го типа. [16]
Реакция образования неопентилгликоля в присутствии гидроокиси натрия протекает в 1 6 раза медленнее, чем при катализе анионитом. При температуре ниже 20 С побочной реакции превращения формальдегида по реакции Канниццарс - Тищенко не наблюдалось. Это согласуется с данными, приведенными выше для превращения чистого формальдегида по реакции Канниццаро - Тищенко. [17]
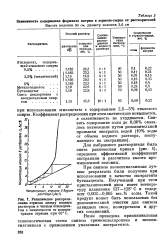 |
Зависимость содержания форниата натрия в этриоле-сырце от растворителей.| Равновесное распреде - продукт может быть использован без. [18] |
При синтезе неопентилгликоля лучшие результаты были получены при использовании в качестве экстрагента бутилацетата. [19]
При выделении неопентилгликоля из водного раствора вода полностью удаляется азеотропной отгонкой с растворителем. Из горячего раствора выделяется формиат натрия, который отфильтровывают. Затем кристаллы диола отфильтровывают; маточный раствор повторно концентрируют ( на 50 %) - выделяются маточные кристаллы диола, после чего отгоняют весь растворитель. В сухом остатке содержатся побочные продукты конденсации и некоторое количество диола, которое определяется методом газо-жидкостной хроматографии. [20]
Для получения чистого неопентилгликоля требуется перекристаллизация или дистилляция. [21]
Возможность применения технического неопентилгликоля для синтеза сложноэфирных смазок резко упрощает технологическую схему его получения ( см. схему IX на стр. [22]
Дихлорэтан плохо растворяет неопентилгликоль на холоду и хорошо - при повышенных температурах ( 50 С), что должно обусловить высокую селективность его как экстрагента. Действительно, использование дихлорэтана в качестве экстрагента позволило выделить из реакционного раствора неопентилгликоль высокой чистоты, не требующий дополнительной перекристаллизации. [23]
Замена этиленгликоля на неопентилгликоль в ненасыщенных полиэфирных смолах, применяемых как связующее в стеклопластиках, повышает теплостойкость и улучшает физико-механические свойства последних. [24]
Подобно этриолу, неопентилгликоль, синтезированный в присутствии щелочей, должен быть отделен от образовавшихся в процессе синтеза формиатов щелочных металлов. [25]
По экстракционной схеме чистый неопентилгликоль может быть получен не только кристаллизацией из концентрированного экстракта, но и ректификацией неопентилгликоля-сырца. Таким образом, экстракционная схема с применением бутил-ацетата в качестве экстрагента позволяет получать чистый неопентилгликоль. [26]
Более высокие выходы неопентилгликоля были получены конденсацией изомасляного альдегида и формальдегида в водном растворе с использованием больших избытков изомасляного альдегида. При этом после гидрирования органической фазы одновременно с неопентилгликолем получают изобутанол. Альдольную конденсацию проводят в водном растворе при 9 - 15 С, мольном соотношении изомасляного альдегида и формальдегида ( 3 18 - - 3 53): 1 и концентрации щелочи 0 27 - 0 19 вес. Гидрирование реакционной смеси производят на медно-хромово-бариевом катализаторе. При этом выход неопентилгликоля составил 80 - 92 %, а изобутанол а - 93 - 96 % от теоретического на взятый изомасляный альдегид. [27]
Впервые промышленное производство неопентилгликоля было организовано в 1957 г. в США фирмой Eastman Chemical Products. [28]
Получение комплексного эфира неопентилгликоля, дикарбоновой кислоты и одноатомного спирта проводится по первому варианту синтеза комплексных эфиров: на первой стадии осуществляют взаимодействие дикарбоновой кислоты и неопент / лгликоля, полученный промежуточный продукт затем этерифицируют одноатоаным спиртом. [29]
Сравнение свойств эфиров неопентилгликоля, метриола и этриола, полученных на основе двух различных смесей кислот С6 - С8, показывает, что по вязкостно-температурным свойствам и термоокислительной стабильности лучше ведут себя эфиры метриола и этриола из кислот, полученных окислением твердых парафинов. [30]
Страницы: 1 2 3 4