Несоответствие - экспериментальные данные
Cтраница 2
Вопросу растворимости нефтепродуктов в воде посвящено сравнительно небольшое число работ. При этом приводимые данные в ряде случаев недостаточно аргументированы и значительно различаются между собой. Основная причина расхождения полученных результатов связана с применением различных методик проведения исследований как в постановке опытов, так и при определении концентраций нефтепродуктов. Несоответствие экспериментальных данных может быть обусловлено также различием углеводородного состава однотипных нефтепродуктов, полученных из разного исходного сырья. [16]
Из изложенного следует, что с помощью методов, основанных на уравнении Дюгема-Маргулеса, можно не только проверить опытные данные, но и в определенных пределах исправить их. Однако эти методы обладают определенными недостатками. При расчете коэффициентов активности на их величину оказывают влияние не только погрешности определения составов равновесных фаз, но также погрешности измерения температуры кипения или давления, так как в выражения для определения f входят, кроме составов фаз, давления паров компонентов при температуре кипения раствора и давление. Это затрудняет решение вопроса об источнике погрешности, вызывающем несоответствие экспериментальных данных уравнению Дюгема-Маргулеса. Рассмотренные методы использования этого уравнения позволяют оценить термодинамическую согласованность опытных данных в целом. [17]
Из изложенного следует, что с помощью методов, основанных на уравнении Дюгема-Маргулеса, можно не только проверить опытные данные, но и в определенных пределах исправить их. Однако эти методы обладают определенными недостатками. При расчете коэффициентов активности на их величину оказывают влияние не только погрешности определения составов равновесных фаз, но также погрешности измерения температуры кипения или давления, так как в выражения для определения у входят, кроме составов фаз, давления паров компонентов при температуре кипения раствора и давление. Это затрудняет решение вопроса об источнике погрешности, вызывающем несоответствие экспериментальных данных уравнению Дюгема-Маргулеса. Рассмотренные методы использования этого уравнения позволяют оценить термодинамическую согласованность опытных данных в целом. [18]
Но именно тогда, когда Планк с воодушевлением изучал ранние работы этих корифеев науки, они, как и многие другие физики, потеряли к термодинамике всякий интерес. Широкая сфера приложения термодинамики, простота ее основ привели их к заключению, что здесь уже все сделано. Они считали, что если и осталось еще что-нибудь в физике неизвестным, то оно кроется в несоответствии экспериментальных данных теоретическим выводам или в теории, которая не является такой логически изящной и строгой, как термодинамика, Короче говоря, в то время большинство физиков считали, что здание термодинамики уже возведено и что оно совершенно по своей форме. Планку законы термодинамики представлялись ключом от бесчисленного количества дверей, ведущих в неизвестное. [19]
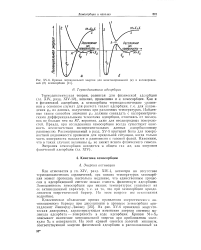 |
Кривые потенциальной энергии для неактивированной ( а и активированной ( б хемосорбции. [20] |
Термодинамическая теория, - развитая для физической адсорбци-и ( гл. XIV-12), конечно, применима и к хемосорбции. Как и в физической адсорбции, в хемосорбции термодинамические уравнения в основном служат для расчета теплот адсорбции, т.е. для нахождения qst из данных, полученных при различных температурах. Найденные таким способом значения qst должны совпадать с калориметрическими дифференциальными теплотами адсорбции, отличаясь от последних не больше чем на RT, вероятно, даже для неоднородных поверхностей. Правда, при исследовании хемосорбции всегда существует опасность несоответствия экспериментальных данных адсорбционному равновесию. XV - 5 критерий Бика для поверхностной подвижности применим для предельной ситуации, когда только часть поверхности находится в равновесии с газовой фазой. Напомним, что в таких случаях величины qst не имеют ясного физического смысла. [21]
Страницы: 1 2