Нитрат - литий
Cтраница 1
Нитрат лития LiNO3 изоморфен с нитратом натрия; легко растворим в воде и спирте. [1]
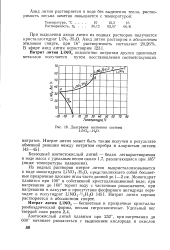 |
Диаграмма состояния системы LiNO3 - Н2О. [2] |
Нитрат лития LiN03 - бесцветные и прозрачные кристаллы ромбоэдрической формы, весьма гигроскопичные. [3]
Нитрат лития легко растворим в воде с небольшим выделением тепла: при растворении 1 моля LiNO3 в 100 молях Н2О при 18 выделяется 300 кал. [4]
Нитрат лития сильно диссоциирован в водном растворе. [5]
Нитрат лития легко растворим в жидком аммиаке и во многих органических растворителях. [6]
Нитрат лития, использованный для приготовления этих катализаторов, имел тенденцию испаряться до разложения, и содержание Li2O в образцах определяли спек-трофотометрически после таблетирования. Все образцы, содержащие Li2O, в пределах точности опытов были каталитически неактивны. Однако поверхность образца ZnO, прокаленного при 1000, составляла 0 086 м21г, тогда как поверхность образца с добавкой LiaO, прокаленного при 700, равнялось 0 136 м2 / г. Первый из них был каталитически активным, а второй - неактивным. При прибавлении около 0 5 % Li активность на единицу поверхности уменьшалась при дегидрогенизации бутена в 5 раз и при разложении бутадиена приблизительно в 15 раз. [7]
Нитрат лития LiNO3 образуется при растворении карбоната лития в азотной кислоте с последующим выпариванием. Нитрат лития - бесцветное кристаллическое вещество, плотность 2 4, плавится при 252 С. LiNOs гигроскопичен, хорошо растворяется в воде с небольшим выделением тепла. [8]
Нитрат лития LiNO3 весьма гигроскопичен, хорошо растворяется в воде, во многих органических растворителях ( этаноле, ацетоне, пиридине) и в жидком аммиаке. В водном растворе легко образует пересыщенные растворы; сильно диссоциирован. При температуре выше 60 С выделяется в виде безводной соли, ниже 60 С - в виде кристаллогидрата. [9]
Для нитратов лития и калия получены кривые растворимости в зависимости от концентрации перекиси водорода с четкими разрывностями. Измерения электропроводности показывают, что эти соли диссоциируют в перекиси водорода так же, как и в воде, но электропроводность кислот в перекиси водорода ниже, чем в воде, что, вероятно, нужно объяснить меньшей подвижностью водородного иона в перекиси водорода. Измерения электропроводности использованы и для обнаружения реакции кислот или солей с перекисью водорода с образованием перекисных соединений. Доказано существование ряда аддитивных соединений с перекисью водорода. Некоторые ссылки, приведенные в табл. 58, относятся к этим пероксигидратам; дальнейшее обсуждение этого вопроса и ссылки па эту и другую литературу приведены в гл. Лишь очень небольшое число таких систем изучено достаточно подробно для представления полных фазовых диаграмм. [10]
Под еоисаждением нитрата лития и других примесей 1ы понимаем общий их переход в твердую фазу незави-имо от того, каким путем он осуществляется. Сокристал-шзацией же будем называть захват примесей, связанный с их внедрением непосредственно в кристаллическую решетку. [11]
В растворах нитрата лития образуются нитратные комплексы лантаноидов и актиния, которые можно разделить на анионите в нитратной форме. [12]
Электропроводность и вязкость системы нитрат лития - метиловый спирт. [13]
Далее была использована смесь нитрата лития и SE-30 и получено лучшее разделение на этой смешанной фазе, чем при использовании индивидуальной SE-30, хотя результат и не был полностью удовлетворительным. [14]
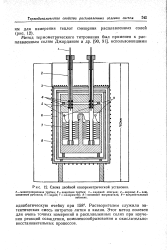 |
Схема двойной калориметрической установки. [15] |
Страницы: 1 2 3 4