Нитрат - литий
Cтраница 2
Растворителем служила эвтектическая смесь нитратов лития и калия. Этот метод полезен для очень точных измерений в расплавленных солях при изучении реакций осаждения, комплексообразования и окислительно восстановительных процессов. [16]
Обсуждается механизм захвата примесей нитратом лития на основани данных по диэлектрической приницаемости и диэлектрическим потерям пол. Сделан вывод, что этим механизмом является обр; зование истинных твердых растворов органической концентрации. [17]
Среди нитратов щелочных элементов только нитрат лития образует кристаллогидрат 1лМОзфЗН2О, а среди нитратов элементов ПА-группы - только Ва ( МОз) 2 кристаллизуется в безводном состоянии. [18]
Кроме того, перхлорат и нитрат лития обладают более высокой плотностью, вполне удовлетворительны в отношении показателей токсичности и коррозионного действия, они также весьма стабильны, если защищены от воздействия воды. [19]
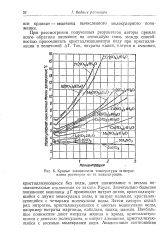 |
Кривые зависимости температуры затвердевания растворов от их концентрации. [20] |
Значительно большее понижение величины ДГ производит нитрат лития, кристаллизующийся с двумя молекулами воды, и нитрат кальция, кристаллизующийся с четырьмя молекулами воды. Затем следует целый ряд нитратов, кристаллизующихся с шестью молекулами воды, например нитраты марганца, кобальта, цинка, магния. Наибольшее понижение дают нитраты железа и хрома, кристаллизующиеся с девятью молекулами, и нитрат алюминия, кристаллизующийся с восемью молекулами воды. [21]
Вудхед показал, что при введении нитрата лития их концентрации увеличиваются. Это явление следует изучить более детально. [22]
 |
Типичные спектры нитратов щелочных металлов в интервале длин волн для полосы поглощения минимальной энергии. [23] |
При переходе от нитрата цезия к нитрату лития наблюдаются существенные изменения длины волны и интенсивности полосы минимальной энергии. [24]
Из 1 М азотной кислоты, насыщенной нитратом лития, экстрагируется при равных объемах фаз 84 % скандия, см. Bock R. [25]
В данном параграфе приводятся исследования по совместному соосаждению нитратов лития, железа и никеля с азотнокислым цезием. [26]
Фоновым электролитом в этом случае служила эвтектическая смесь нитратов лития, натрия и калия. [27]
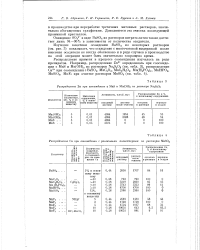 |
Распределение Zn при соосаждении с MnS и Мп ( ОН2 из раствора Na2S208.| Распределение Са при соосаждении с различными коллекторами из растворов MnS04. [28] |
Осаждение S04a - в виде BaS04 из растворов нитрата лития также достигает лишь 94 - 96 % в зависимости от количества осадителя. [29]
Указанный метод применен при изучении предельного пересыщения растворов нитратов лития, цезия и бария, а также тетраборнокислого натрия. При этом установлено, что получаемые значения предельных пересыщений аналогичны по величине тем, которые определялись другими методами. [30]
Страницы: 1 2 3 4