Нитрат - щелочной металл
Cтраница 1
Нитраты щелочных металлов легкоплавки и хорошо растворимы в воде. Если NaCl плавится при температуре 808 С, то температура плавления NaNO3 равна 310 С. [1]
Нитраты щелочных металлов ( NaNO3, KNO3) при нагревании выделяют в свободном состоянии лишь V3 содержащегося в них кислорода. Обычно кислород получают из хлората калия. [2]
Нитраты щелочных металлов и аммония при температурах до 125 или совсем не гидролизуются водой или гидроли-зуются очень слабо, так что концентрация получающейся азотной кислоты будет очень низкой, вследствие чего эти соли не дают нитросоединений при нагревании их растворов с углеводородами. [3]
Нитраты щелочных металлов обычно называют селитрами: NaNO3 - чилийская селитра, KNO3 - калийная селитра. [4]
Нитраты щелочных металлов и аммония при температурах до 125 или совсем не гидролизуются водой или гидролизуются очень слабо, так что концентрация получающейся азотной кислоты будет очень низкой, вследствие чего эти соли не дают нитросоединений при нагревании их растворов с углеводородами. [5]
Нитраты щелочных металлов являются сильными окислителями. С некоторыми веществами способны образовывать взрывоопасные смеси. [6]
Хлориды и нитраты щелочных металлов реагируют с BrF5 непосредственно, a KJ, NH4C1 и NH3 - даже загораются. [7]
Бинарные смеси нитратов щелочных металлов на этом же рисунке обозначены треугольниками, а бинарные и тройные смеси нитратов щелочных металлов с нитратами поливалентных катионов - кружочками. Все приведенные данные либо непосредственно измерены при 360, либо получены экстраполяцией для этой температуры. [8]
Как плавни, нитраты щелочных металлов имеют преимущества перед другими солями: они легкоплавки, нелетучи, малоагрессивны. [9]
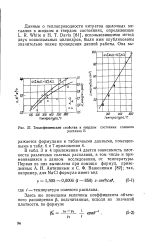 |
Теплофизические свойства в твердом состоянии солевого. [10] |
Данные о теплопроводности нитратов щелочных металлов в жидком и твердом состояниях, определенные L. R. White и Н. Т. Davis [81], использовавшими метод двух коаксиальных цилиндров, были ими опубликованы значительно позже проведения данной работы. [11]
Раствор хлоридов или нитратов щелочных металлов обрабатывают в колбе избытком щавелевой кислоты при нагревании на водяной бане. [12]
Раствор хлоридов или нитратов щелочных металлов обрабатывают в колбе избытком щавелевой кислоты при нагревании на водяной бане Вначале реакция идет довольно медленно, но когда температура дость гает примерно 100 С, она становится бурной и в случае необходимости должна быть замедлена охлаждением раствора. Раствор выпаривают досуха, прибавляют немного воды и, если требуется, повторяют выпаривание, следя за тем, чтобы в смеси всегда находился избыток щавелевой кислоты. Под конец остается смесь щавелевой кислоты и оксалатов, которые могут быть осторожным прокаливанием переведены в карбонаты. [13]
Для смесей с нитратами щелочных металлов ( кроме LiNOg) это уравнение, как показали наши расчеты, выполняется плохо. [14]
Для смесей с нитратами щелочных металлов ( кроме LiNO3) это уравнение, как показали наши расчеты, выполняется плохо. [15]
Страницы: 1 2 3 4