Нитрат - торий
Cтраница 1
Нитрат тория является важнейшей его солью, имеющей практическое значение. Подобно нитратам РЗЭ, нитрат тория диссоциирует при нагревании с образованием сперва основных солей, затем чистой окиси тория. Процесс начинается при температуре 125 С и заканчивается при 360 С. [1]
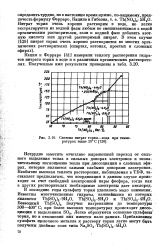
Нитрат тория довольно хорошо растворим в воде, вплоть до очень высоких температур. Его равновесная диаграмма растворимости приведена на рис. 4.1. Как видно на рисунке, при высоких температурах растворимость весьма высокая, причем она увеличивается с повышением температуры. Одна из проблем - испарение НМОз и продуктов ее разложения из растворов при повышенных температурах. Поэтому для получения постоянного избытка НМОз она должна непрерывно добавляться к раствору, а пары не должны выводиться из системы. Другой проблемой является гидролитическая нестабильность растворов, содержащих более 65 % Th ( NO3) 4, при температурах выше 225 С и выпадение из них белого осадка. [2]
Нитрат тория может экстрагироваться из водных растворов многими органическими экстрагентами. В литературе по аналитической химии описано большое число таких экстрагентов, но единственным экстрагентом, широко применяемым в химических процессах ( см. раздел 10.5), является трибутилфосфат. Таким образом, экстракция протекает более полно, если концентрация Th ( NO3) 4 высока. Для более эффективной экстракции тория из ЕСДНЫХ растворов необходимо создать более благоприятные, чем для урана, условия экстракции: иметь более высокие концентрации ТБФ в растворителе и высаливающих агентов в водной фазе. При низких концентрациях ТБФ уран экстрагируется, а торий остается в водной фазе. На рис. 4.2 показано, что коэффициенты распределения между НМО3 и раствором ТБФ урана и тория в области низких концентраций весьма подходящи для их разделения. [3]
Нитрат тория был выделен из водных растворов в виде кристаллов с переменным числом гидратационной роды. Ферраро, Кацин и Гибсон [133] идентифицировали Th ( NO3) 4 - 4H2O, Th ( NO3) 4 - 5H2O и Th ( N03) 4 - 6H20, причем наиболее устойчивым из них оказался пента-гидрат. [4]
 |
Система Th ( NO4 - HNO - Н 0 при температуре 25 С. [5] |
Нитрат тория был выделен как кристаллическое твердое вещество с переменным количеством гидратационной воды. Фер-раро, Кацин и Гибсон [125] идентифицировали Th ( N03) 4 - 4H2O, Th ( N03) 4 - 5H2O и Th ( N08) 4 - 6H2O, при этом наиболее устойчивым оказался пентагидрат. [6]
 |
Система нитрат тория-вода при температурах выше 20Ъ С. [7] |
Нитрат тория очень хорошо растворим в воде, но легко экстрагируется из водной фазы любым не смешивающимся с водой органическим растворителем, если к водной фазе добавить азотную кислоту или другой растворимый нитрат. [8]
Нитрат тория экстрагируется значительно лучше, когда большая часть азотной кислоты в водной фазе будет заменена нитратами, например нитратом натрия, кальция или алюминия. Это хорошо видно из данных табл. 4, взятых в работе Мак-Кея. [9]
Нитрат тория используют при кондук-тометрическом определении фторидов, кремнефтористово-дородной кислоты и комплексных соединений, образованных BF3 с пиридином, диметилнитрозоамином и пиколи-ном. Определения основаны на выделении осадка ThF-i. Титрование фторидов проводят в 50 % - ном этаноле. [10]
Нитрат тория - белое кристаллическое вещество, хорошо растворимое в воде и этаноле. [11]
Облученный нитрат тория ( 10 мккюри) растворяют в 6 мл 8 М соляной кислоты. [12]
Нитрат тория Th ( NO3) 4 12Н2О очень хорошо растворим в воде и спирте. Он также растворим в эфире, содержащем азотную кислоту. [13]
Растворимость нитрата тория в воде при 25 С составляет 65 6 вес. Безводный нитрат растворяется также в эфирах, спиртах и кетонах. Водный раствор Th ( NO3) 4 имеет кислую реакцию вследствие гидролиза. Гидраты нитрата тория отщепляют воду при температуре ниже 100 С. Выше 150 С происходит разложение Th ( NO3) 4 с выделением окислов азота. [14]
Раствор нитрата тория ( 0 03 мг / мл) смешивают с раствором арсеназо III в отношении 2: 3, непосредственно перед употреблением. [15]
Страницы: 1 2 3 4