Нитрат - редкоземельный элемент
Cтраница 1
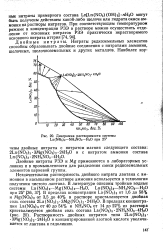 |
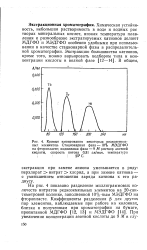
Диаграмма растворимости системы La ( N 3 3 - NH4NO3 - H2O при 25. [1] |
Нитраты редкоземельных элементов способны образовывать двойные соединения с нитратами аммония, щелочных, щелочноземельных и других металлов. [2]
Раствор нитратов редкоземельных элементов, содержащий 25 мл азотной кислоты и не более 0 15 г СеО2, разбавляют до 75 мл, прибавляют 0 5 г бромата калия и перемешивают до его растворения. Затем медленно при непрерывном перемешивании вводят раствор иодата калия ( 10 г иодата и 33 3 мл азотной кислоты в 100 мл) в 10 - 15-кратном количестве по отношению к теоретически необходимому для связывания находящегося в растворе церия. Кидкости дают стечь и немедленно смывают осадок с фильтра обратно в стакан. Разминают комки, взбалтывают смесь, снова фильтруют и дают жидкости стечь. После этого опять смывают осадок в стакан, на этот раз применяя около 50 мл горячей воды, нагревают до кипения и, непрерывно перемешивая, по каплям вводят азотную кислоту до растворения осадка. [3]
Раствор нитратов редкоземельных элементов, содержащий 25 мл азотной кислоты и не более 0 15 г Се02, разбавляют до 75 мл, прибавляют 0 5 г бромата калия и перемешивают до его растворения. Затем медленно при непрерывном перемешивании вводят раствор иодата калия ( 10 г иодата и 33 3 мл азотной кислоты в 100 мл) в 10 - 15-кратном количестве по отношению к теоретически необходимому для связывания находящегося в растворе церия. Жидкости дают стечь и немедленно смывают осадок с фильтра обратно в стакан. Разминают комки, взбалтывают смесь, снова фильтруют и дают жидкости стечь. После этого опять смывают осадок в стакан, на этот раз применяя около 50 мл горячей воды, нагревают до кипения и, непрерывно перемешивая, но каплям вводят азотную кислоту до растворения осадка. [4]
Галогениды и нитраты редкоземельных элементов и иттрия очень хорошо растворяются в воде. [5]
Нейтральный раствор нитратов редкоземельных элементов разбавляют до 200 мл и кипятят с 5 г бромата натрия; когда начнут появляться пары брома, вносят несколько маленьких кусочков ( величиной с горошину) чистого мрамора1 и кипячение продолжают в течение нескольких часов, периодически дабавляя горячую воду для пополнения убыли от испарения. После того, как несколько капель профильтрованного раствора дадут отрицательную реакцию на церий с перекисью водорода ( см. разд. VIII), извлекают мрамор, осадок отфильтровывают, промывают 2 % - ным раствором азотнокислого натрия и растворяют в азотной кислоте в присутствии нескольких капель перекиси водорода. Полученный раствор выпаривают досуха и осаждение повторяют. Объединенные фильтраты кипятят с броматом и кусочком мрамора и, если выделится еще осадок, то его очищают повторным осаждением. [6]
Для опытов были приготовлены растворы нитратов редкоземельных элементов и иттрия, исходя из наиболее чистых окислов, проверенных спектральным анализом. Окислы растворяли в концентрированной HNOa при нагревании и удаляли избыток последней упариванием на водяной бане. [7]
Для опытов были приготовлены растворы нитратов редкоземельных элементов и иттрия, исходя из наиболее чистых окислов, проверенных спектральным анализом. Окислы растворяли в концентрированной HNOs при нагревании и удаляли избыток последней упариванием на водяной бане. [8]
На рис. 4 показано разделение миллиграммовых количеств нитратов редкоземельных элементов на 20-сантиметровой колонке, заполненной 10 % - ным МЭДГФО на фторопласте. [10]
Так, молярные коэффициенты поглощения хлоридов или нитратов редкоземельных элементов составляют от единиц до нескольких десятков; молярные коэффициенты поглощения растворов простых солей меди, никеля и хрома ( III) составляют 100 - 200 единиц. Таким образом, фотометрические методы, основанные на измерении собственного светопоглощения гидратированных ионов некоторых металлов, как правило, обладают малой чувствительностью. Прежде всего, такие методы требуют очень мало времени для выполнения анализа. В этом случае необходимо время только для наполнения кюветы и проведения измерения. Второе преимущество состоит в том, что не требуется расходовать реактивы. Но главное достоинство метода заключается в легкости применения автоматики в контроле производства, так как в данном случае по пути движения жидкости или газа необходимо лишь установить фотоэлемент и освещать его через слой контролируемых жидкости или газа светом с определенной длиной волны. Показания фотоэлемента записывают с помощью автоматических самописцев. Так можно определять содержание окислов азота при проведении различных процессов, содержание основного компонента в ваннах никелирования, меднения или хромирования, а также многие другие компоненты, которые поглощают свет IB доступной для иосле-дова Н ИЯ области помощью простой аппаратуры. [11]
Полученные в результате экстракционного разделения азотнокислые водные растворы нитратов редкоземельных элементов и тория обрабатывают в соответствии со способом дальнейшего использования очищенных препаратов. Например, действием NH4OH могут быть выделены соответствующие гидроокиси или действием щавелевой кислоты - оксалаты. [12]
При введении в равновесие эквимолярных количеств Na2NiL и нитрата редкоземельного элемента Ьп ( ЫОз) з ионы редкоземельных элементов, конкурируя с ионами никеля за комплексообразующий агент, вытесняют из комплекса никель. Поэтому для каждого раствора полярограмма получается с двумя волнами. [13]
Другой метод разделения основан на небольшой, но различной растворимости нитратов редкоземельных элементов в органических растворителях. Фус и Вильгельм [35] подробно описали метод разделения лантаноидов жидкостной экстракцией с трибутилфоефатом. [14]
 |
Кривые потенциометрического титрования смесей солей, смесей солей с кислотами, смесей солей с основаниями в среде метилэтилкетона. [15] |
Страницы: 1 2