Нитрид - индий
Cтраница 2
С помощью указанного комплекса аппаратуры изучены карбиды титана, циркония, гафния, ванадия, ниобия, тантала, хрома бора; бориды лантана, церия, празеодима, неодима, самария, гадолиния, иттербия, титана, циркония, ниобия, тантала, железа; сульфиды лантана, церия, празеодима, неодима, самария, европия, гадолиния, иттербия, гафния, тантала, хрома, молибдена, вольфрама; нитриды индия, скандия, лантана, самария, титана, циркония, гафния, ниобия, бора, алюминия, германия, галлия, кремния, фосфора; селениды лантана, празеодима, неодима, самария, европия; силициды хрома, лантана; фосфиды празеодима и неодима. [16]
Желтый нитрид галлия получается при пропускании аммиака над нагретым до 1000 С галлием, а также в результате разложения ( NH4) 3 [ GaF6j в атмосфере аммиака. Нитрид индия получен аналогичным образом из ( NH4) 3 [ InF6 ] при более низкой температуре. Остальные пниктогениды получают синтезом из компонентов. [17]
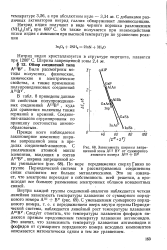 |
Зависимость ширины запрещенной зоны A111 BV от суммарного атомного номера АШ BV. [18] |
С добавками различных активаторов нитрид галлия обнаруживает люминесценцию. Нитрид индия получают в виде черного порошка разложением ( NH4) 3InF6 при 600 С. [19]
Как показали опыты, металлический индий не взаимодействует с аммиаком при температуре 300 - 1000 С. Была проведена серия опытов по выяснению получения нитрида индия восстановлением - азотированием его окиси аммиаком. Реакция восстановления окиси индия с одновременным азотированием индия In2O3 2NH3 - 2InN 3H2O протекает до температуры 600 С очень медленно. При дальнейшем повышении температуры до 640 С наблюдается частичное разложение индия. Таким образом, интервал температур, в котором образуется нитрид индия состава, близкого к расчетному, очень узок и составляет 620 - 630 С. [20]
В противоположность нитриду индия, фосфат индия имеет свойства полупроводника, несмотря на наличие у него структуры цинковой обманки, очень приближающейся к структуре вюрцита нитрида индия. Может быть, что такая аномалия обусловлена влиянием примесей, и поэтому нитрид индия нуждается в дальнейшем изучении. Согласно сообщению Ньюмена, особенности нитрида индия, возможно, обусловлены присутствием свободного индия. Это предположение подкрепляется тем, что запретная зона нитрида индия составляет 2 4 эв. [21]
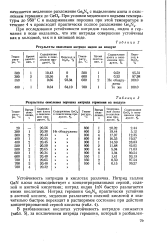 |
Результаты окисления нитрида индия на воздухе.| Результаты окисления порошка нитрида германия на воздухе. [22] |
Устойчивость нитридов в кислотах различна. Нитрид галлия GaN плохо взаимодействует с концентрированными серной, соляной и азотной кислотами; нитрид индия InN быстро разлагается этими кислотами. [23]
 |
Зависимость ширины запрещенной зоны соединений A1UBV от суммарного атомного номера компонентов. [24] |
Исключительно важны пниктогениды элементов подгруппы галлия самые важные полупроводниковые соединения типа A111 Bv, Висмут такие соединения не образует. Желтый нитрид галлия получается при пропускании аммиака над нагретым до 1000 С галлием, а также в результате разложения ( NH4) JGaFJ в атмосфере аммиака. Нитрид индия получен аналогичным образом из ( NH4) JInF jl при более низкой температуре. Остальные пниктогениды получают прямым синтезом из компонентов. [25]
Висмут такие соединения не образует. Желтый нитрид галлия получается при пропускании аммиака над нагретым до 1000 С галлием, а также в результате разложения ( ГШ4) з [ СаГб ] в атмосфере аммиака. Нитрид индия получен аналогичным образом из ( РШ4) з [ 1пГ6 ] при более низкой температуре. Остальные пниктогениды получают синтезом из компонентов. [26]
В противоположность нитриду индия, фосфат индия имеет свойства полупроводника, несмотря на наличие у него структуры цинковой обманки, очень приближающейся к структуре вюрцита нитрида индия. Может быть, что такая аномалия обусловлена влиянием примесей, и поэтому нитрид индия нуждается в дальнейшем изучении. Согласно сообщению Ньюмена, особенности нитрида индия, возможно, обусловлены присутствием свободного индия. Это предположение подкрепляется тем, что запретная зона нитрида индия составляет 2 4 эв. [27]
В противоположность нитриду индия, фосфат индия имеет свойства полупроводника, несмотря на наличие у него структуры цинковой обманки, очень приближающейся к структуре вюрцита нитрида индия. Может быть, что такая аномалия обусловлена влиянием примесей, и поэтому нитрид индия нуждается в дальнейшем изучении. Согласно сообщению Ньюмена, особенности нитрида индия, возможно, обусловлены присутствием свободного индия. Это предположение подкрепляется тем, что запретная зона нитрида индия составляет 2 4 эв. [28]
Как показали опыты, металлический индий не взаимодействует с аммиаком при температуре 300 - 1000 С. Была проведена серия опытов по выяснению получения нитрида индия восстановлением - азотированием его окиси аммиаком. Реакция восстановления окиси индия с одновременным азотированием индия In2O3 2NH3 - 2InN 3H2O протекает до температуры 600 С очень медленно. При дальнейшем повышении температуры до 640 С наблюдается частичное разложение индия. Таким образом, интервал температур, в котором образуется нитрид индия состава, близкого к расчетному, очень узок и составляет 620 - 630 С. [29]
Через трубку пропускают интенсивный поток NHs, высушенногс над металлическим натрием. Когда температура печи достигнет 630 С, лодоч ку вдвигают в горячую зону трубки. Температуру доводят до 580 - 600 С i выдерживают в этих условиях в течение 15 мин. Затем за 10 мин температур) снижают до 520 С и сохраняют эту температуру еще 10 мин до полного удаления NH4F из препарата. Более медленное повышение температуры и длительг ное нагревание приводят к частичной потере азота нитридом индия. [30]
Страницы: 1 2 3