Нитрид - литий
Cтраница 2
Найденные нами условия синтеза нитрида лития путем взаимодействия металлического лития с азотом позволяют быстро получать чистый препарат без расплавления или тонкого измельчения металла и без очистки азота. [16]
Солеобразными ( ионными) являются нитриды лития, магния и меди. [17]
Кроме L1N, известны также нитрид лития Li3N, имид лития LiNH3 амнд лития LiNH2, азид лития LiNs, нитрид лития LiNO2, нитрат лития LiNOs. Взаимодействие лития с водой происходит без плавления и самовозгорания с образованием гидроксида LiOH я выделением водорода. При непосредственном взаимодействии расплавленного лития с водородом образуется гидрид LiH. С сухнм кислородом при низкой температуре не реагирует. [18]
При нагревании в атмосфере водорода нитрид лития переходит в гидрид с одновременным образованием аммиака. Наоборот, несколько более сильным нагреванием гидрида в атмосфере азота может быть получен нитрид. [19]
Кинетические кривые для процесса образования нитрида лития аналогичны кривым автокаталитических реакций: образование нитрида лития вначале идет крайне медленно, затем скорость реакции возрастает, достигая максимального значения, после чего падает до нуля. Реакция взаимодействия лития с азотом относится к типу топохимических реакций. [20]
 |
Кристаллическая решетка и свойства ионных нитридов. [21] |
Примечание: Т - ра плавления нитрида лития ( L13N) дана под давлением азота. [22]
Результаты, полученные при исследовании взаимодействия нитридов лития и бария с азотом, находятся в соответствии с оценками энергий образования высших нитридов этих элементов по методу проф. [23]
Все они сходны по свойствам с нитридом лития, но гораздо менее устойчивы. Так, Na - jN медленно разлагается на элементы уже при 200 С, а нитриды К, Rb и Cs даже взрывчаты. [24]
Составьте формулы следующих соединений: а) нитрида лития ( соединения лития с азотом); б) сульфида алюминия ( соединения алюминия с серой); в) фторида фосфора, в которых электроположительный элемент проявляет максимальную степень окисления. [25]
При непосредственном взаимодействии с азотом легко образуется только устойчивый нитрид лития: 6Li N22LiaN, при 250 С взаимодействие значительно ускоряется. [26]
По МРТУ 6 - 09 - 1105 - 64 нитрид лития должен содержать не менее 35 % азота и не более 0 05 % примеси железа. Практически изложенный метод дает продукт, содержащий не менее 38 % азота ( по теории 40 %) и не более 0 02 % железа. Содержание других примесей зависит от качества исходного металла. [27]
Аммиак, образовавшийся при гидролизе смеси нитрида кальция и нитрида лития, в которой массовая доля азота равнялась 30 0 %, пропустили через 80 мл раствора бромоводородной кислоты. [28]
Все они более или менее сходны по свойствам с нитридом лития, но гораздо менее устойчивы. Так, NasN медленно разлагается на элементы уже при 200 С, а нитриды К, Rb и Cs даже взрывчаты. Следует отметить, что имеющиеся данные по ннтри 1ам тяжелых щелочных металлов не очень надежны. [29]
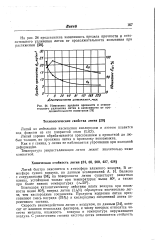 |
Изменение предела прочности и относительного удлинения лития в зависимости от продолжительности испытания. [30] |
Страницы: 1 2 3 4