Нитрид - литий
Cтраница 3
Благодаря каталитическому действию влаги воздуха при влажности менее 80 % нитрид лития ( LijN) образуется значительно легче, чем кислородные соединения. Продукты коррозии лития представляют смесь нитрида ( 75 %) и кислородных соединений лития переменного состава. [31]
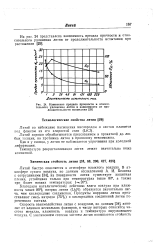 |
Изменение предела прочности и относительного удлинения лития в зависимости от продолжительности испытания. [32] |
Благодаря каталитическому действию влаги воздуха при влажности менее 80 % нитрид лития ( Li3N) образуется значительно легче, чем кислородные соединения. Продукты коррозии лития представляют смесь нитрида ( 75 %) и кислородных соединений лития переменного состава. [33]
При комнатной температуре азот инертен и соединяется только с литием, образуя нитрид лития ( стр. [34]
Кинетические кривые для процесса образования нитрида лития аналогичны кривым автокаталитических реакций: образование нитрида лития вначале идет крайне медленно, затем скорость реакции возрастает, достигая максимального значения, после чего падает до нуля. Реакция взаимодействия лития с азотом относится к типу топохимических реакций. [35]
Скорость коррозии в литии сильно увеличивается под влиянием примесей, среди которых особой агрессивностью отличается нитрид лития. [36]
В качестве катализаторов Венторф называет кальций, магний, барий, литий, олово и нитрид лития. [37]
При комнатной температуре N2 реагирует только с литием ( во влажной атмосфере), образуя нитрид лития Li3N; нитриды других элементов синтезируют при сильном нагревании, например, такие как Mg3N2 и BN. Пассивность газообразного азота используют для создания инертной атмосферы при проведении химических реакций между веществами, чувствительными к кислороду. [38]
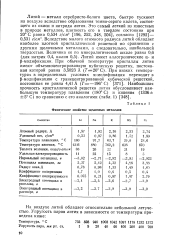 |
Физические свойства щелочных металлов. [39] |
Литий - металл серебристо-белого цвета, быстро тускнеет на воздухе вследствие образования темно-серого налета, состоящего из окиси и нитрида лития. Вследствие малого атомного радиуса литий обладает наиболее плотной кристаллической решеткой по сравнению с другими щелочными металлами, а следовательно, наибольшей твердостью. Литий имеет аллотропические а - и р-модификации. [40]
Кроме L1N, известны также нитрид лития Li3N, имид лития LiNH3 амнд лития LiNH2, азид лития LiNs, нитрид лития LiNO2, нитрат лития LiNOs. Взаимодействие лития с водой происходит без плавления и самовозгорания с образованием гидроксида LiOH я выделением водорода. При непосредственном взаимодействии расплавленного лития с водородом образуется гидрид LiH. С сухнм кислородом при низкой температуре не реагирует. [41]
Аргон обычно используется в тех случаях, когда азот нежелателен из-за его реакционной способности, например в реакциях с применением лития может образоваться нитрид лития. Аргон рекомендуется применять при реакциях активных металлов, требующих нагревания. Поскольку аргон тяжелее воздуха, он очень эффективен для заполнения систем; при подаче в систему аргон заполняет ее снизу, вытесняя воздух в верхнюю часть. [42]
Напишите формулы следующих соединений: карбонат кальция, карбид кальция, гидрофосфат магния, гидросульфид натрия, нитрат железа ( III), нитрид лития, гидроксикарбонат меди ( II), дихромат аммония, бромид бария, гексацианоферрат ( II) калия, тетрагидроксиалюминат натрия, декагидрат сульфата натрия. [43]
Гидрид лития весьма реакционноспособен: очень бурно реагирует с водой; с жидким аммиаком взаимодействует с образованием амида, а с газообразным - лишь при 320 С; с кислородом, хлором и азотом при обычной температуре не взаимодействует, но при нагревании с азотом образует нитрид лития, с хлором и хлористым водородом - хлорид лития. При длительном нагревании до 650 - 700 С LiH взаимодействует с серой, углеродом, кремнием и фосфором с образованием сульфида, карбида, силицида и фосфида лития соответственно. Гидрид лития образует двойные гидриды ( алюмогидрид, борогидрид и др.), которые широко используются в аналитической химии и для органического синтеза. [44]
Соединения электроположительных элементов с элементами главных подгрупп V, IV и III групп периодической системы - азотом, фосфором, мышьяком, сурьмой, углеродом, кремнием и бором - называют по международной номенклатуре нитридами, фосфидами, арендами ( арсенидами), стибидами ( антимо-нидами), карбидами, силидами ( силицидами), боридами: Li3N - нитрид лития, MgsAs2 - аренд магния. [45]
Страницы: 1 2 3 4