Нитрид - натрий
Cтраница 1
Нитрид натрия, Na3N, получают, пропуская газообразный аммиак через нагретый металлический натрий или подвергая действию электрических разрядов металлический натрий в атмосфере азота. [1]
Нитрид натрия Na3N был получен действием на натрий сильных электрических разрядов в атмосфере азота. [2]
Нитрид натрия разлагается при 300 С, нитрид алия еще менее прочен, а нитриды рубидия и цезия, по-видимому, не образуются при обычных температурах. [3]
Нитрид натрия устойчив в сухом воздухе, но моментально разлагается водой или спиртом с образованием аммиака. [4]
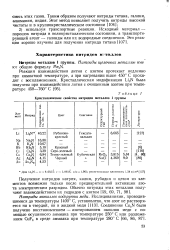 |
Кристаллические свойства нитридов металлов I группы. [5] |
Получение нитридов натрия, калия, рубидия и цезия из элементов возможно только после предварительной активации азота электрическим разрядом. [6]
Для предохранения труб от коррозии при межоперационноы хранении их обрабатывают в растворе нитрида натрия. [7]
При растворении продукта в воде образуются NH3, ОН и N2, по-видимому, вследствие гидролиза нитрида натрия. В спектре облученного азида наблюдается новая полоса поглощения при 3400 А, которая, вероятно, является / - полосой, обусловленной аннигиляцией экситонов на анионных вакансиях. Квантовый выход весьма высок, около 0 25, а тепловая энергия активации имеет низкое значение, примерно равное 0 5 ккал / моль. [8]
При температурах, превышающих 300 С, где удобных масел нет, используется смесь равных частей нитрата калия и нитрида натрия. Такая смесь хорошо работает в интервале от 150 до 600 С. Смеси этих солей весьма коррозионно активны, поэтому термостаты и все детали, которые контактируют с горячей солью, должны быть сделаны из коррозионно стойкого материала, например из нержавеющей стали. Необходимо подчеркнуть, что контакт воды или влаги с расплавленной солью дол - жен категорически исключаться, так как даже самые малые их количества могут быть причиной серьезного взрыва. Важно также избежать контакта с расплавленной солью любого легкоокисляющегося материала, например алюминия. Перед сборкой или началом эксплуатации соляного термостата необходимо ознакомиться с промышленной инструкцией по технике безопасности, предписывающей меры предосторожности при работе с нитратными соляными ваннами. [9]
На Златоустовском заводе после зачистки прутки вновь травят и в отличие от технологии, используемой на других заводах, погружают на 2 - 3 мин в 20 % - ный водный раствор нитрида натрия, нагретый до 70 - 80 С. Образовывающийся при этом на поверхности прутков тонкий налет нитрида натрия служит хорошим подслоем для смазки при волочении и обеспечивает стойкость волок. Этот способ подготовки прутков к волочению требует соблюдения мер предосторожности и связан с некоторым увеличением расходов по переделу. [10]
В жидкую среду добавляют ингибитор коррозии ( 1 % - ный раствор кальцинированной соды), после обработки стальные детали во избежание вторичной коррозии промывают в 0 2 % - ном растворе хромпика или нитрида натрия. Однако наличие водорастворимых солей на поверхности детали резко ухудшает защитные свойства лакокрасочных покрытий, поэтому рекомендуется непосредственно после операции гидропескоструйной очистки детали подвергнуть пассивации. [11]
В жидкую среду добавляют ингибитор коррозии ( 1 % - ный раствор кальцинированной соды), после обработки стальные детали во избежание вторичной коррозии промывают в 0 2 % - ном растворе хромпика или нитрида натрия. Однако наличие водорастворимых солей на поверхности детали резко ухудшает защитные свойства лакокрасочных покрытий, поэтому рекомендуется непосредственно после операции гидропескоструйной очистки детали подвергнуть пассивации. [12]
Почему при взаимодействии нитрида натрия с водным раствором щелочи происходит более интенсивное выделение аммиака, нежели при взаимодействии его ( нитрида) с водой. [13]
Натрий легко образует соединения с серой - Na2S и Na2S2, которые применяются в технике, в частности при обработке кожи. Соединение натрия с азотом - нитрид натрия Na3N, в отличив от нитрида лития, образуется лишь при повышенной температуре. [14]
При определении в олове, ниобии, титане, бериллии и сталях водород отгоняют при 1100 С в вакууме с применением аргона в качестве газа-носителя и окисляют оксидом меди ( II) до воды. Воду переводят в аммиак с помощью нитрида натрия. [15]
Страницы: 1 2 3