Нитрид - цирконий
Cтраница 3
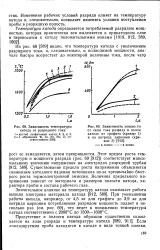
При уменьшении работы выхода, например, от 4 5 эв для графита до 2 9 эв для нитрида циркония потребляемая разрядом мощность падает в несколько раз ( см. рис. 69), что ведет к понижению температуры катода соответственно с 2000 С до 1500 - 1600 С. [32]
При возможном химическом взаимодействии термопары с исследуемым веществом рабочая часть проволоки изолируется оболочкой, например, из ванадия, нитрида циркония или вольфрама. [33]
При построении диаграммы состояния для карбида циркония ZrCo923 нами была принята температура плавления, равная 3400 С [4], а нитрида циркония ZrNo. Эта температура значительно отличается от таковой по диаграмме состояния Zr - ZrN, предложенной Домогала [8], однако, принимая во внимание предположительный характер границ фазовых полей ( ZrN - f а) тв - ZrNTB и ( ZrN жидкость) - ZrNTB на этой диаграмме и наши экспериментальные данные, ее следует принять именно такой. Все остальные точки получены непосредственно из эксперимента. [34]
Сплавы с такой структурой являются естественными композиционными материалами, в которых пластичная металлическая матрица армирована тугоплавкими и высокопрочными волокнами и пластинами нитрида циркония. В заэвтектических сплавах уменьшается количество эвтектики и появляются крупные избыточные кристаллы нитрида циркония. [35]
Какие из перечисленных ниже соединений могут иметь достаточно широкую область гомогенности: окислы вольфрама, окись магния, двуокись кремния, сульфид циркония, нитрид циркония, закись меди, трехокись сурьмы. [36]
Область высокотемпературного азотирования циркония ( 900 - 1600 С) исследована автором работы [ 61, в которой найдено, что наряду с р-твердым раствором азота в цирконии образуются внешние тонкие пленки из a - твердого раствора и нитрида циркония. [37]
Если процесс ведут в присутствии азота, то карбид всегда содержит примесь азота. Нитрид циркония получают действием азота на порошкообразный цирконий при 800 - 1000 С или действием газообразного аммиака на четыреххлористый цирконий. [38]
 |
Давление пара металла над нитридами титана и циркония. [39] |
Кнудсена измерены давления пара металла над некоторыми составами нитридов титана и циркония. Состав нитрида циркония изменяется даже пои испарении в эффузионном режиме Кнудсена. [40]
Это различие может быть обусловлено разной концентрацией валентных электронов в рассматриваемых соединениях, определяемых как общее число всех внешних электронов компонентов соединения. Для нитрида циркония стехиометрического состава концентрация валентных электронов равна 9 или 4 5 эл / апгом ( так же, как для NbC и ТаС), а для нитрида ниобия - 5 эл / апгом. Отклонение от стехиометрического состава снижает электронную концентрацию. Интересно отметить, что Тк нитрида ниобия у нижней границы области гомогенности кубической фазы ( около состава NbN 82), которой отвечает электронная концентрация около 4 5 эл / апгом, почти соответствует Тк нитрида циркония стехиометрического состава, характеризующегося таким же значением электронной концентрации. [41]
В твердом нитриде циркония заряды ионов не Зе, а значительно меньше. [42]
Цирконат свинца в виде твердого раствора с титанатом свинца используют для пьезоэлектрической керамики. Карбид и нитрид циркония в небольших количествах применяют для изготовления твердых сплавов. Тетра-хлорид циркония предложено использовать в качестве компонента катализаторов для полимеризации олефинов. Оксихлорид и окси-нитрат циркония идут на приготовление катализаторов в производстве бутадиена из спирта и в других процессах. Большие перспективы имеет применение двойных сульфатов циркония в качестве дубителей кож, где они дают лучшие результаты, чем дубители растительного происхождения. [43]
Цирконат свинца в виде твердого раствора с титанатом свинца используется в качестве материала для пьезокерамики. Карбид и нитрид циркония применяют для изготовления твердых сплавов. [44]
Цирконах свинца в виде твердого раствора с титанатом свинца используется в качестве материала для пьезокерамики. Карбид и нитрид циркония применяют для изготовления твердых сплавов. [45]
Страницы: 1 2 3 4