Нитрогеназа
Cтраница 1
Нитрогеназа легко и даже более эффективно восстанавливает ацетилен, причем избирательно, до этилена. Эта реакция служит подходящим тестом для проверки активности нитрогеназы. [1]
Нитрогеназа - фермент, ответственный за восстановительную фиксацию азота с образованием аммиака бактериями и сине-зелеными водорослями. Этот процесс осуществляется при атмосферном давлении, при обычных температурах и в среде, содержащей большое количество воды. В противоположность этому, промышленный способ связывания азота ( габеровский процесс) основан на применении высоких температур и давлений. Способность микроорганизмов восстанавливать в мягких условиях вещество, которое по традиции рассматривалось как в высшей степени химически инертное, привлекла к нитрогеназным ферментам значительный интерес. Этот интерес базируется не только на желании понять механизм важнейшего биохимического процесса, но и на стремлении построить синтетический катализатор по типу нитрогеназы и найти таким путем новые способы получения соединений азота. [2]
Нитрогеназа является активным ферментом для фиксации азота. Она содержит два белка. Группы Fe4S4 действуют, вероятно, как окислительно-восстановительные центры. Предполагаемое расположение этих компонентов в соответствии с наблюдаемыми свойствами показано на рис. 18.20. Оба белка нитрогеназы сами по себе не проявляют способности фиксировать азот, но рекомбинация их приводит к образованию активной системы со значительным перемещением белковых цепей. [3]
Бактериальная нитрогеназа инактивируется свободным кислородом, поэтому время ее полужизни иа воздухе очень коротко. Это означает, что в процессе эволюции должны были выработаться сложные механизмы, способные обеспечить бактероидам анаэробные условия в клетках корня при достаточном снабжении кислородом самих корней. Rhizobium индуцирует в клетках хозяина синтез леггемоглобина-связывающего кислород белка, аналогичного миоглобину млекопитающих. Молекулы леггемоглобииа, окружая бактероиды, препятствуют избыточному снабжению их кислородом. [5]
В отсутствие N2 нитрогеназа катализирует вьщеление молекулярного водорода в реакции, протекающей с затратой АТФ. [6]
 |
Switch-off - эффект ионов.| Работа нитрогеназного комплекса. [7] |
В отсутствие N2 нитрогеназа интенсивно выделяет Н2, так как электроны восстановителей необходимо сбросить. [8]
Специфические приспособления для защиты нитрогеназы от высоких концентраций 02 выработаны симбиотическими азотфик-саторами - клубеньковыми бактериями. [9]
Как отмечалось ранее, нитрогеназа крайне чувствительна к кислороду. [10]
Данные, полученные для бактериальной нитрогеназы, свидетельствуют об активации молекулярного азота ионами металла. Существенными компонентами бактериальной системы фиксации азота считаются молибден, негемовое железо и кислотно-лабильные сульфиды, поэтому естественно, что большая часть попыток построить химические модели нитрогеназы была основана на предположении, что железо и молибден - ключевые элементы фиксации азота. В отсутствие внешних субстратов и в меньшей степени при наличии субстратов в присутствии нитрогеназы наблюдается выделение водорода. Поскольку ацетилен одновременно является конкурентным ингибитором фиксации азота и потому предполагается, что он связывается с активным центром фермента, его неоднократно использовали в качестве удобного субстрата для испытания нитрогеназной активности как нативного фермента, так и его химических моделей. Адекватность модели нитрогеназы может быть окончательно установлена по ее способности катализировать восстановление молекулярного азота при комнатной температуре и обычном давлении. [11]
Некоторые ученые обнаружили, что нитрогеназа, помимо восстановления азота до иона аммония, может катализировать восстановление ряда субстратов. Такие оценочные исследования показали, что штаммы Rhizobium широко варьируют по способности фиксировать азот и стимулировать рост бобовых. Бертон и др. показали, что некоторые растения-хозяева способны сотрудничать с широким спектром ризобактерий, тогда как другие высокоспецифичны, вступая в активные симбиотические отношения только с одним штаммом Rhizbium - Внутри кросс-инокулирую-щих групп некоторые виды бобовых сходным образом отвечают на инокуляцию определенных штаммов ризобактерий. Это впоследствии првело к выработке эффективного группирования, и изготовители инокулятов смогли производить и предлагать ннокуляты для многих хозяев наряду со специфическими нно-кулятами. [12]
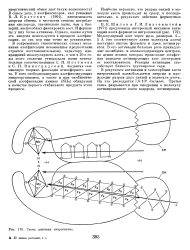 |
Схема действия нитрогеназы. [13] |
В результате активации и хемосорбции азота нитрогеназой высвобождается энергия и происходит разрыв двух связей в молекуле азота. На это расходуется 7 8 - 105 дж / моль. [14]
Нежелательная побочная реакция фиксации азота - восстановление нитрогеназой Н до Н2 ( газообразный водород), в ходе которой энергия ( в форме АТР) расходуется на образование водорода, который в конечном счете просто улетучивается. В результате только от 40 до 60 % всего потока электронов, проходящих через нитрогеназныи комплекс, передается на N2, что значительно уменьшает эффективность процесса фиксации азота. В принципе, если бы Н2 мог превратиться обратно в Н, потери энергии были бы ниже, и процесс фиксации азота стал бы более эффективным. Устранить же эту побочную реакцию прямым путем невозможно, поскольку она обусловлена особенностями химического строения активного центра нитрогеназы, и если попытаться блокировать ее, изменив структуру фермента, то неизбежно произойдет и уменьшение активности нитрогеназы. [15]
Страницы: 1 2 3 4
