Бензодиазин
Cтраница 1
Все незамещенные бензодиазины представляют собой низкоплавкие кристаллические вещества, растворимые в воде и органических растворителях. Также как и в нафталине, в бензодиазинах существует заметная локализация связей в циклических системах: связи 1 2 и 3 4 обладают характером двойной, а связь 2 3 - одинарной связей. [1]
У-Оксиды бензодиазинов, как правило, вступают во все реакции, характерные для этой серии диазинов. [2]
 |
Синтетические подходы к хииоксалииам и фталазииам. [3] |
Химия бензодиазинов во многом схожа с химией моноциклических аналогов; в частности, заместители при атомах углерода гетероциклического кольца испытывают активирующее влияние атомов азота. Некоторые главные аспекты химии бензодиазинов рассмотрены ниже. [4]
Химические свойства бензодиазинов легко предвидеть, но естественно, что определенные члены ряда отличаются от других аналогов своим специфическим характером. Это положение хорошо иллюстрируют примеры из химии хиназолина. Все бензо-диазины относительно устойчивы, однако хиназолин разлагается при нагревании с водными растворами кислот и щелочей на бензальдегид и муравьиную кислоту. [5]
Электрофильное замещение бензодиазинов в целом не очень широко исследовано, однако можно оценить некоторые общие тенденции. Диазины без активирующих заместителей не подвергаются электрофильному замещению. В бензодиазинах имеются доступные атаке положения в бензольном кольце; там возможно и действительно происходит замещение, хотя и в жестких условиях. [6]
Электрофильное замещение бензодиазинов в целом не очень широко исследовано, однако можно оценить некоторые общие тенденции. Дпазины без активирующих заместителей не подвергаются электрофилыюму замещению. В бензодназинах имеются доступные атаке положения в бензольном кольце; там возможно и действительно происходит замещение, хотя и в жестких условиях. [7]
А - Оксиды бензодиазинов, как правило, вступают во все реакции, характерные для этой серии диазинов. [8]
 |
Синтетические подходы к хииоксалииам и фталазииам. [9] |
Электрофильное замещение для бензодиазинов нехарактерно. Все изомерные бензодиазины нитруются смесью азотной и серной кислот в карбоциклическое кольцо. Замещение протекает в катионах бензодиазинов. [10]
Реакции прямого нуклеофильного замещения бензодиазинов, например аминирования, не описаны. По всей вероятности, это объясняется тем, что замещенные бензодиазины легче получить другими методами. [11]
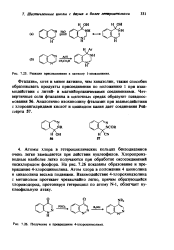 |
Реакции присоединения к катиону 1-хииазолииия.| Получение и превращение 4-хлороциииолииа. [12] |
Атомы хлора в гетероциклических кольцах бензодиазинов очень легко замешаются при действии нуклеофилов. Хлоропроиз-водные наиболее легко получаются при обработке оксосоединений оксихлоридом фосфора. На рис. 7.26 показаны образование и превращение 4-хлороциннолина. Атом хлора в положении 4 циннолина и хиназолина весьма подвижен. Взаимодействие 4-хлорохиназолина с метанолом протекает чрезвычайно легко, причем образующийся хлороводород, протонируя гетероцикл по атому N-1, облегчает ну-клеофильную атаку. [13]
Хиноксалины образуют W-оксиды легче любых других представителей бензодиазинов ( ср. Заместители в положениях 2 и 3 влияют так же, как и в случае других бензодиазинов. [14]
Протоны алкильных групп в а - или уположении к кольцевому Анатому бензодиазинов имеют кислый характер ( ср. Эти карбанионы участвуют во многих реакциях, характерных для активных метнленовых соединений. Мстилциннолин при конденсации с бензальдегидом с хорошим выходом дает 4-стирилциннолии ( 194), но не реагирует или дает полимерные продукты со многими производными бенз-альдегида, например салициловым альдегидом и п-нитробенз-альдегидом. Реакции этого типа катализируются хлоридом цинка, однако в ряду циннолина он почти не влияет на выход продуктов. [15]
Страницы: 1 2 3