Нитротиофен
Cтраница 2
Данные о том, что при нитровании 2-нитротиофена образуется смесь изомеров, содержащая 80 - 85 % 2 4-динитрозамещенного 96, 97 ], несомненно ошибочны: авторы судили о соотношении образовавшихся изомеров по количеству выделенных продуктов в к тому же использовали в качестве исходного нитротиофен, содержащий, как теперь известно ( см. выше), - 15 % 3-изомера. Значительная примесь последнего неизбежно должна была приводить к существенному увеличению количества 2 4-динитрозамещенного в продукте реакции. Быть может, наиболее сильным классическим ориентантом II рода, который в заметной степе -: ни, хотя далеко не полностью, способен преодолеть эффект гетероатома, является сульфониевая группа. Изученное нами [79] нитрование солей диметил-2 - тиенилсульфония дает 4 - и 5-изомеры в соотношении - 2: 1; подробнее этот вопрос рассмотрен ниже. [16]
Тиофен - ароматический гетероцикл, более реакционноспособ-ный в отношении злектрофилов, чем бензол, и менее, чем пиррол и фуран. Нитротиофены и подобные им соединения восприимчивы к атакам нуклеофилов. [17]
Гетероциклические соединения, обладающие ароматическим характером, при действии азотной кислоты могут быть превращены в соответствующие нитропроизводные. Мейер и Штадлер23 получили нитротиофен посредством пропускания воздуха, насыщенного парами тиофена, через дымящую азотную кислоту, причем на 1 объем тиофена затрачивалось 4 объема азотной кислоты. По окончании опыта реакционную смесь разбавляли водой и собравшееся над водным слоем масло отделяли и перегоняли с водяным паром. [18]
Гетероциклические соединения, обладающие ароматическим характером, при действии азотной кислоты могут быть превращены в соответствующие нитроыроизводные. Мейер и Штад-лер [49] получили нитротиофен посредством пропускания воздуха, насыщенного парами тиофена, через дымящую азотную кислоту, причем на 1 объем тиофена затрачивалось 4 объема азотной кислоты. По окончании опыта реакционную смесь разбавляли водой и собравшееся над водным слоем масло отде-ляли и перегоняли с водяным паром. Продуктами реакции оказались мононитротиофен ( т, пл. [19]
Гетероциклические соединения, обладающие ароматическим характером, при действии азотной кислоты могут быть превращены в соответствующие нитроыроизводные. Мейер и Штад-лер [49] получили нитротиофен посредством пропускания воздуха, насыщенного парами тиофена, через дымящую азотную кислоту, причем на 1 объем тиофена затрачивалось 4 объема азотной кислоты. По окончании опыта реакционную смесь разбавляли водой и собравшееся над водным слоем масло отделяли и перегоняли с водяным паром. Продуктами реакции оказались мононитротиофен ( т, пл. [20]
Замедление полимеризации стирола в присутствии нитротиофена гораздо более заметно, чем в присутствии нитробензола. Задержка происходит, невидимому, из-за реакции растущего свободного радикала полимерной цепи с нитротиофеном, причем ядро тиофена более активно взаимодействует со свободным радикалом, чем бензольное кольцо. Радикал атакует свободное и наиболее активное а-иоложение тиофена. [21]
Слабым иш ибиторным действием обладают также летучие ингибиторы, относящиеся к веществам с окислительными свойствами. Сюда относятся органические эфиры азотистой кислоты, нитрозамины, ни-тросоединения, в частности нитрофенолы и нитротиофены. Для обеспечения эффективной защиты требуется большая концентрация этих веществ, одновременно рН поверхностной пленки на металле должен быть достаточно высоким. [22]
Металлирование облегчается при добавлеьи. ТМЭДА или при использовании мощных ненуклео-фильных оснований, например диизопропиламида лития, с помощью которого даже бром - и нитротиофены можно достаточно избирательно металлировать при - 70 С. [23]
При взаимодействии с хлором, бромом или с ацетатом ртути все водороды тиофена могут быть замещены на галоген или на ртуть. Хотя тиофен можно нитровать в подходящих условиях, однако обычно он реагирует с крепкой азотной кислотой очень бурно, претерпевая разложение. Нитротиофены при восстановлении превращаются в соответствующие аминопроизводные, однако 2 - и 3-аминотиофены устойчивы лишь в отсутствие воздуха. [24]
Раствор 42 г тиофена в 170 мл уксусного ангидрида медленно прибавляют к смеси 40 г дымящей азотной кислоты ( уд. По окончании реакции оставляют стоять реакционную массу в течение 2 час. Нитротиофен выделяется в виде светложелтых кристаллов. Его отсасывают, промывают ледяной водой, отжимают и сушат в эксикаторе. При перекристаллизации из петролейного эфира получают 2-нитротиофен с т, пл. [25]
При взаимодействии с хлором, бромом или с ацетатом ртути все водороды тиофена могут быть замещены на галоген или на ртуть. Хотя тиофен можно нитровать в подходящих условиях, однако обычно он реагирует с крепкой азотной кислотой очень бурно, претерпевая разложение. Нитротиофены при восстановлении превращаются в соответствующие аминопроизводные, однако 2 - и 3-аминотиофены устойчивы лишь в отсутствие воздуха. [26]
Нитробензол получают прямым нитрованием бензола. Наиболее вероятными примесями являются нитропроизводные циклических соединений, содержащихся в качестве примесей в бензоле. Чаще всего это - нитротолуол и нитротиофен. [27]
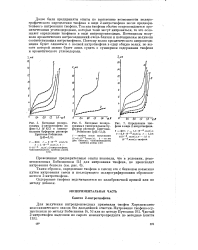
Далее были предприняты опыты по выяснению возможности полярографического определения тиофена в виде 2-нитротиофена после предварительного нитрования тиофена. Так как тиофены обычно сопровождаются ароматическими углеводородами, которые тоже могут нитроваться, то это осложняет определение тиофенов в виде нитропроизводных. Потенциалы полу-волн ароматических нитросоединений очень близки к потенциалам полуволн соответствующих нитротиофенов. [29]
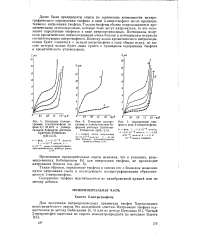 |
Определение тиофена в виде 2-нитротиофена.| Катодные подпрограммы 2-нитротиофена на фоне 0 1 М KG1 в универсальном буферном растворе Бриттона-Робинсона ( рН2 0. [30] |
Страницы: 1 2 3