Обезвоживание - кристаллогидрат
Cтраница 1
Обезвоживание кристаллогидратов и другие термохимические превращения хлорида кобальта подробно исследованы с помощью термографических и термогравиметрических методов. [1]
Обезвоживание кристаллогидрата следует проводить при температуре, немного превышающей температуру его разложения 1разл - ту температуру, при которой давление пара Ь О над кристаллогидратом равно 101 3 кПа ( 1 атм. При / с tpa3JI обезвоживание идет очень медленно, при / 3 1разл наряду с удалет нием воды могут протекать и другие процессы. [2]
Для обезвоживания кристаллогидратов по последнему методу в стеклянный стакан помещают мелкорастертую соль и заливают ее ацетоном. Стакан плотно закрывают пробкой, в которую вставлен тонкий капилляр для отвода водорода и других газов. Обезвоживание протекает через жидкую фазу: кристаллизационная вода отщепляется и диффундирует в жидкость, из которой она удаляется за счет взаимодействия с осушителем. Дегидратация длится в течение нескольких дней. [3]
Для обезвоживания кристаллогидратов этим методом в стеклянный стакан помещают мелкорастертую соль и заливают ее ацетоном. [4]
Для обезвоживания кристаллогидратов по третьему методу в стеклянный стакан помещают мелкорастертую соль и заливают ее ацетоном. [5]
Для обезвоживания других кристаллогидратов требуется довольно сильное нагревание. [6]
При обезвоживании кристаллогидратов имеет место гидролиз хлоридов с образованием нерастворимых в воде окси-хлорндов [4], поэтому обезвоживание проводят в условиях, предотвращающих гидролиз. Для этого используют хлористый водорот, хлористый тионил, четыреххлористый углерод, хлористый аммоний, монохлорид серы и другие. [7]
При обезвоживании кристаллогидратов под действием концентрированных растворов, на изотерме растворимости появятся участки, отвечающие первичной кристаллизации кристаллогидрата В х Н20 и безводного компонента В. Структура диаграммы растворимости этого типа ( рис. 204) также должна быть понятной читателю без специальных пояснений. [9]
При обезвоживании кристаллогидрата Na2SOs хН2О он, превращаясь в безводную соль, теряет половину своего веса. [10]
При обезвоживании кристаллогидратов солей часто наблюдается гидролиз. Степень гидролиза определяется отношением числа гцдролизован-ных молекул к общему числу молекул вещества. [11]
При обезвоживании кристаллогидрата двухлори-стой меди из 1 023 г кристаллогидрата получено 0 807 г безводного хлорида меди. Сколько молекул воды приходится на одну молекулу безводной соли. [12]
Дальше происходит обезвоживание кристаллогидрата и выпадение соли АХ. При этом испаряющаяся вода восполняется водой, отдаваемой кристаллогидратом, так что состав раствора не меняется. Система в это время трехфаз-на и, поскольку температура и давление постоянны, не имеет степеней свободы. В точке Е раствор насыщен кристаллами АХ и ВХ, и при испарении воды его состав больше не изменится. [13]
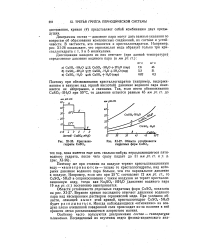 |
Области устойчивости гидратных форм CuSO4. [14] |
Поэтому при обезвоживании кристаллогидратов ( например, выдерживанием в вакууме, над серной кислотой) давление водяного пара изменяется не непрерывно, а скачками. [15]
Страницы: 1 2 3 4
