Обезвоживание - кристаллогидрат
Cтраница 2
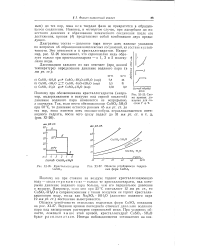 |
Области устойчивости гидрат-ных форм CuSO4. [16] |
Поэтому при обезвоживании кристаллогидратов ( напри - Рис xj 25 Схе-мер, выдерживанием в вакууме над серной кислотой) ма кривых да-давление водяного пара изменяется не непрерывно, вления для си-а скачками. [17]
Указание [25 ] о легком обезвоживании кристаллогидратов фтористого кобальта и никеля ошибочно. [18]
Сразу же активно начинается обезвоживание кристаллогидрата с выделением большого количества теплоты. Безводная соль в виде тонких белых кристаллов оседает на дно стакана. [19]
Аналогично можно рассмотреть процесс обезвоживания кристаллогидратов. [20]
Как и во всех случаях сушки и обезвоживания кристаллогидратов или растворов, сульфат натрия, выходящий из аппаратов кипящего слоя, получается в гранулированном виде со сравнительно низким содержанием мелких фракций. [21]
 |
Термограммы с записью электропроводности для CuSO4 5НаО ( а и CoSO4 7Н2О ( б. [22] |
В настоящей работе приводятся результаты исследования процессов обезвоживания кристаллогидратов с одновременной регистрацией на пирометре термических эффектов и электропроводности. [23]
Препарат, почти не содержащий воды, получите многочасовым обезвоживанием соответствующего кристаллогидрата при 300 С. Препарат SrO2 - 0 68 H2O получите обработкой при 55 С раствора 5 г Sr ( NO3) 2 в 5 мл 30 % - го Н2О2 7 мл 25 % - го раствора аммиака. [24]
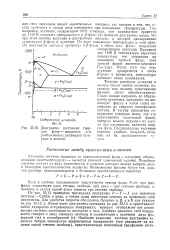 |
Диаграмма состояния твердая фаза - жидкость для изделия разбавленных растворов угле - вая их рода в железе. гула. [25] |
Удаление летучего вещества из кристаллической фазы - например, обезвоживание кристаллогидрата - является обычной химической задачей. Подобные системы состоят из двух компонентов, в качестве которых можно выбрать воду и безводное кристаллическое вещество. [26]
Среди методов получения безводного хлорида магния особое место занимает обезвоживание кристаллогидратов. [27]
 |
Диаграмма состояния твердая фаза - жидкость для изделия разбавленных растворов угле - вая их рода в железе. гуна. [28] |
Удаление летучего вещества из кристаллической фазы - например, обезвоживание кристаллогидрата - является обычной химической задачей. Подобные системы состоят из двух компонентов, в качестве которых можно выбрать воду и безводное кристаллическое вещество. [29]
Дигалиды СоНа12 также образуются при взаимодействии простых веществ или обезвоживанием соответствующих кристаллогидратов. Дигалиды ( кроме CoF2) растворимы в воде. Гидроксид Со ( ОН) 2 существует в виде синей и розовой модификаций. Синяя модификация получается при действии щелочей на соли Со ( II) на холоду; при нагревании Со ( ОН) 2 переходит в розовую модификацию. В воде Со ( ОН) 2 не растворяется. По химической природе он как и СоО, - амфотерное соединение, преимущественно проявляющее основные свойства. [30]
Страницы: 1 2 3 4