Первый обертон - валентное колебание
Cтраница 2
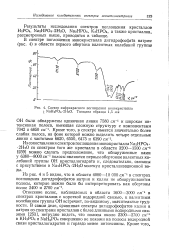 |
Спектр инфракрасного поглощения монокристалла NaH2PO4 - 2HaO. Толщина образца 1 5 мм. [16] |
Из сопоставления спектров поглощения монокристалла Na2HPO4 - 2Н2О со спектром того же кристалла в области 3200 - 3500 см-г [259] можно сделать предположение, что обнаруженные нами у 6380 - 8000 см-1 полосы являются первым обертоном валентных колебаний группы ОН кристаллогидрата и, следовательно, связаны с присутствием в Na2HPO4 - 2HaO молекул кристаллизационной воды. [17]
Первичные ароматические амины являются хорошим примером такого межмолекулярного взаимодействия. В ходе исследования первого обертона валентного колебания NH было найдено [114], что молярный коэффициент поглощения этой полосы меняется от 1 87 в циклогексане до 0 61 в ацетонитриле. В других растворителях получаются промежуточные значения. Этот эффект в данном случае обратен тому, что наблюдалось для соответствующей основной полосы. Ясно, что изменение растворителя в такой системе требует перестройки заново рабочей кривой. [18]
На рис. 84 показано изменение спектра поглощения алюмосиликата при адсорбции на нем анилина. Полоса поглощения ( 6690 см 1) первого обертона валентного колебания групп N - Н анилина, растворенного в СС14, представлена кривой а. Кривая б дает поглощение погруженного в СС14 алюмосиликата. Как видно из кривых в и г рис. 84, увеличение концентрации анилина вызывает ослабление полосы ОН при 7220 см 1 алюмосиликата и появление в спектре полос самого анилина. Полоса поглощения при 5940 см 1 принадлежит колебаниям групп СН молекул анилина. [19]
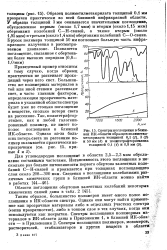 |
Спектры поглощения в ближней ИК-области образцов полиметил-метакрилата толщиной 0 1 ( 1, 3 ( 2 и 50 мм ( 3 и политетрафторэтилена толщиной 0 1 ( 4 и 0 8 мм ( 5. [20] |
Для углеводородов поглощение в области 2 5 - 2 3 мкм обусловлено составными частотами. Интенсивность этого поглощения в несколько раз больше интенсивности первого обертона валентных колебаний С - Н - связей и проявляется при толщинах поглощающего слоя около 200 - 300 мкм. [21]
Наряду с основными частотами колебаний в поглощении участвуют также частоты обертонов и составные частоты. Частоты обертонов кратны основной частоте. Например, первый обертон валентного колебания С - Р связей политетрафторэтилена имеет частоту около 2400 см 1, что соответствует удвоенной частоте основного колебания. [22]
Из спектроскопических данных Киселев и Лыгин ( 1961а) рассчитали колебательную, вращательную и конфигурационную энтропии воды, адсорбированной на гидроксилированной поверхности кремнезема. Для адсорбированной воды были выбраны две модели, в первой из них вода связана водородной связью с одной, - а во второй - с двумя гидроксильными группами. Рассчитанные значения энтропии были меньше, чем экспериментально определенные, что указывает на наличие других степеней свободы подвижности молекул, возможно колебаний параллельно поверхности, дающих вклад в экспериментальные значения энтропии. Аналогичные расчеты были предприняты ( Киселев, Лы-тин, 19616) для случая взаимодействия между поверхностными гидроксильными группами и физически адсорбированным бензолом и к-гексаном. Расчеты энтропии показывают, что м-гексан имеет значительно большую поверхностную подвижность, чем бензол. Эти расчеты согласуются с экспериментальными спектроскопическими и калориметрическими исследованиями, которые указывают на более сильное взаимодействие адсорбированного бензола с поверхностью. Например, Филимонов ( 1956) нашел, что частота первого обертона валентного колебания гидроксильной группы кремнезема смещалась в сторону уменьшения на 236 см-1 и 70 см 1 при адсорбции бензола и к-гексана соответственно. Киселев ( 19616) привел значения теплот адсорбции бензола и к-гексана на гидра-тированной поверхности кремнезема, равные 10 4 и 8 8 ккал / моль соответственно. В расчетах Киселева и Пошкуса ( 1958) было показано, что большее значение теплоты адсорбции бензола обусловлено квадрупольно-дипольной энергией взаимодействия между адсорбированным бензолом и поверхностными гидроксильными группами. [23]
Из спектроскопических данных Киселев и Лыгин ( 1961 а) рассчитали колебательную, вращательную и конфигурационную энтропии воды, адсорбированной на гидроксилированной поверхности кремнезема. Для адсорбированной воды были выбраны две модели, в первой из них вода связана водородной связью с одной, - а во второй - с двумя гидроксильными группами. Рассчитанные значения энтропии были меньше, чем экспериментально определенные, что указывает на наличие других степеней свободы подвижности молекул, возможно колебаний параллельно поверхности, дающих вклад в экспериментальные значения энтропии. Аналогичные расчеты были предприняты ( Киселев, Лыгин, 19616) для случая взаимодействия между поверхностными гидроксильными группами и физически адсорбированным бензолом и w - гексаном. Расчеты энтропии показывают, что к-гексан имеет значительно большую поверхностную подвижность, чем бензол. Эти расчеты согласуются с экспериментальными спектроскопическими и калориметрическими исследованиями, которые указывают на более сильное взаимодействие адсорбированного бензола с поверхностью. Например, Филимонов ( 1956) нашел, что частота первого обертона валентного колебания гидроксильной группы кремнезема смещалась в сторону уменьшения на 236 см - и 70 см 1 при адсорбции бензола и к-гексана соответственно. Киселев ( 19616) привел значения теплот адсорбции бензола и к-гексана на гидра-тированной поверхности кремнезема, равные 10 4 и 8 8 ккал / молъ соответственно. В расчетах Киселева и Пошкуса ( 1958) было показано, что большее значение теплоты адсорбции бензола обусловлено квадрупольно-дипольной энергией взаимодействия между адсорбированным бензолом и поверхностными гидроксильными группами. [24]
Страницы: 1 2