Электронное облако - молекула
Cтраница 1
 |
Строение молекулы воды. [1] |
Электронное облако молекулы, образованное пятью парами электронов, схематически распределено так ( рис. 2 6), что внутренняя пара окружает ядро кислорода, две внешние пары неравномерно поделены между ядрами кислорода и водорода, тяготея больше к кислороду, а остальные две пары кислород не делит с водородом, и их заряды остаются частично нескомпенсированными. Таким образом, в молекуле воды оказывается четыре полюса зарядов: два отрицательных за счет избытка электронной плотности у кислородных пар электронов и два положительных - вследствие недостатка электронной плотности у несколько оголенных ядер водорода - протонов. [2]
Перекрывание электронных облаков молекул сопровождается химическим взаимодействием. Происходит перераспределение электронной плотности и образуется химическая связь, сильная или слабая. [3]
 |
Строение молекулы ЕОДЫ. [4] |
Структура электронного облака молекулы воды показана на рис. 1.1. В молекуле имеется 10 электронов ( 5 пар): одна пара внутренних электронов расположена вблизи ядра кислорода; две пары внешних электронов обобщены попарно между каждым из протонов и ядром кислорода; две остальные пары внешних электронов являются неподеленными, их орбиты направлены к противоположным от протонов вершинам тетраэдра. [5]
При химической реакции электронное облако молекулы перестраивается и действительно возникают бро-мируемые двойные связи. Почему же, спросит осведомленный читатель, вссьмичленное кольцо C8Hs бронируется много легче, чем бензол, совершенно подобно ненасыщенному этиленовому углеводороду. [6]
При химической реакции электронное облако молекулы перестраивается и действительно возникают бро-мируемые двойные связи. Почему же, спросит осведомленный читатель, восьмичленное кольцо С8Н8 бромиру-ется много легче, чем бензол, совершенно подобно ненасыщенному этиленовому углеводороду. [7]
 |
Направленность электронных орбиталей ( а и схема распределения зарядов в молекуле воды ( б. [8] |
Таким образом, электронное облако молекулы воды имеет вид четырех лепестков, направленных к вершинам неправильного тетраэдра. Электронное облако в молекуле воды смещается к атому кислорода, так как он имеет большую электроотрицательность. Вследствие этого вблизи ядер атомов водорода создается избыток положительного заряда. [9]
До тех пор, пока электронные облака молекул endue перекрываются, волновая функция системы в принципе может быть представлена с помощью ( В. [10]
Второй тип предполагает перекрывание электронных облаков взаимодействующих молекул. При этом могут образовываться направленные связи, две или несколько молекул образуют устойчивые ассоциации. Примером является образование молекулярных комплексов за счет водородных связей или сил донорно-акцепторного типа. Второй тип взаимодействий существует не во всех конденсированных системах. [11]
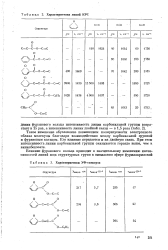 |
Характеристики линий КРС.| Характеристики УФ-спекгров. [12] |
Такое изменение обусловлено повышением поляризуемости электронного облака молекулы благодаря взаимодействию между карбонильной группой и фурановым кольцом. Его влияние передается и на двойную связь. При этом интенсивность линии карбонильной группы оказывается гораздо выше, чем в винилбензоате. [13]
С использованием этих правил симметрия электронного облака молекулы бензола в основном состоянии обозначается символом Aig. [14]
Конечно, при поглощении кванта света электронное облако молекулы перераспределяется, однако при этом возникает не устойчивое, а возбужденное состояние. [15]
Страницы: 1 2 3 4 5