Электронное облако - молекула
Cтраница 4
На рис. 53 представлено взаимодействие электронных облаков атомов водорода с образованием связывающих и разрыхляющих электронных облаков молекулы водорода. На рис. 54 видно, что при взаимодействии р - облаков атомов возникают т - МО, а не тг - МО. [46]
Исследование характера связи на уровне сил, действующих на ядра со стороны различных участков электронного облака молекулы, - это не только наглядный прием, обладающий рядом положительных качеств, о которых уже шла речь выше. Этот подход открывает многообразие деталей и особенностей химической связи в разных рядах соединений, о которых ничего не говорит классическая структурная формула. [47]
Положительный член в выражении (2.19) описывает силы межмолекулярного отталкивания и главным образом обусловлен перекрыванием электронных облаков взаимодействующих молекул. При концентрации электронов в малой области понижается ассоциированная с ними волна де Брой-ля, а так как р / гД, то при понижении А, возрастает р ( импульс), а следовательно, увеличивается кинетическая энергия электронов, что и приводит к отталкиванию. Гиршфельдер и Букингем ( 1956) показали, что силы межмолекулярного отталкивания описывает член вида F ( г) е - Вг, где F ( r) полином от г, а В - положительный параметр. [48]
 |
Формы простейших молекул. [49] |
Выше ( § 7) уже было указано, что при образовании чисто ковалентной связи электронное облако молекулы, возникающее в результате перекрывания электронных облаков одинаковых атомов, занимает симметричное положение между остовами соединяющих атомов. [50]
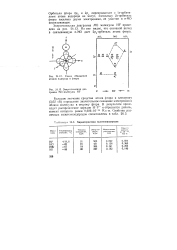 |
Схема сближения атомов водорода и фтора.| Энергетическая диаграмма МО молекулы HF.| Характеристики галогеноводородов. [51] |
Большое значение сродства атома фтора к электрону ( 3 62 эВ) определяет значительное смещение электронного облака молекулы в сторону фтора. [52]
 |
Депарафинизация дизельного топлива в присутствии различных активато. [53] |
Активность активаторов, а следовательно и механизм их действия определяется строением, размерами и распределением электронных облаков молекул. [54]
Может возникнуть вопрос: достаточно ли велико время взаимодействия между ионом и молекулой для того, чтобы электронное облако молекулы сместилось под влиянием поля пролетающего иона столь же сильно, как и под действием постоянного электрического поля равной величины. S сек; это время достаточно велико для того, чтобы сместить электронное облако из равновесного положения. [55]
Величина поляризуемости молекул имеет порядок 1 A3 ( lA3 10 - 30 м3) и характеризует объем электронного облака молекулы. Эта наглядность утрачивается в системе СИ, где [ а ] Кл ма / В. Поляризуемость, связанная с деформацией частицы, называется деформационной. [56]
На свойства жидкостей и р аотворов неэлектролитов наибольшее влияние оказывают слабые химические взаимодействия, возникающие при перекрывании электронных облаков молекул. При этом широко используются оптические, радиофизические, рентгенографические, хроматографические, акустические и другие методы. [57]
В твердых растворах или смесях эти процессы могут происходить но обменно-резонансному механизму, для осуществления которого необходимо перекрывание электронных облаков молекул, что происходит на расстояниях порядка 10 А. Возможен также индуктивно-резонансный перенос энергии электронного возбуждения от молекул в триплетном состоянии к молекулам, у которых спектр поглощения перекрывается спектром фосфоресценции молекулы, передающей энергию. При таком механизме передача энергии может осуществляться на расстоянии порядка 50 А. [58]
При поляризации молекул в электрическом поле высокой частоты возникает индуцированный дипольный момент молекулы ( ( л), который обусловлен смещением электронного облака молекул. В статических полях или полях с относительно низкими частотами колебаний происходит поляризация вещества в целом, включающая небольшое смещение ядер и преимущественную ориентацию молекул вдоль поля. Экспериментально измеряемые в электрическом поле величины связаны с индуцированными дипольными моментами, из которых можно определить постоянный дипольный момент молекулы цо. [59]
Универсальной составной частью молекулярных сил являются дисперсионные силы, обусловленные наличием у любой молекулы мгновенных диполей, возникающих в результате флуктуации плотности электронного облака молекул и атомов. [60]
Страницы: 1 2 3 4 5