Область - пассивность
Cтраница 1
Область пассивности во всех растворах электролитов незначительна. [1]
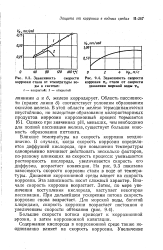 |
Зависимость скорости коррозии стали от температуры воды в системе.| Зависимость скорости. [2] |
Область пассивности ( правее линии б) соответствует условиям образования окислов железа. Однако при значениях рН, меньших, чем необходимо для полной пассивации железа, существует большая опасность образования петтинга. [3]
В области неполной пассивности ( между потенциалами пассивации и Фладе-потенциалом) электрохимическое поведение деформируемого электрода - определяется двумя совместно действующими факторами: механохимическим эффектом и пассива-ционными явлениями, осложненными механическими напряжениями. [4]
В области неполной пассивности ( между потенциалами пассивации и Фладе-потенциалом) электрохимическое поведение деформируемого электрода определяется двумя совместно действующими факторами: механохимическим эффектом и пассивационными яв - лениями, осложненными механическими напряжениями. [5]
Однако установление области пассивности только на основании значений растворимостей продуктов коррозионной реакции, как это делается на подобных диаграммах, не будет в действительности вполне определенным. Следует иметь в виду, что образование нерастворимых или, точнее, малорастворимых продуктов реакции не всегда означает фактическое установление пассивного состояния и невозможность протекания коррозионного процесса. Примером может быть отсутствие пассивности и, наоборот, заметная скорость ржавления железа в нейтральных растворах, содержащих хлор-ионы, несмотря на весьма малую растворимость конечных продуктов реакции. Для возникновения электрохимической пассивности металла необходимым условием является не вообще возможность образования нерастворимых продуктов коррозии, а только образования их в результате анодного процесса непосредственно на реагирующей поверхности, а не в растворе вследствие вторичных процессов между анодными и катодными продуктами кор-розионной реакции. [6]
Участок CD соответствует области устойчивой пассивности металла. Обычно плотность тока растворения на этом участке практически не зависит от потенциала. [8]
Нашим традиционным направлением в области пассивности является сравнительное изучение электрохимического поведения пассивных металлов и их окислов. Это направление представлено в разделах, посвященных молибдену, титану, платине, кобальту и никелевым сплавам. Кроме того, в книгу включены результаты исследования механизма действия кислородсодержащих анионов СгО -, МпО и C10J на кинетику растворения пассивного железа в сернокислых растворах. Помимо обычного потенциостатическог метода, в1 этой работе использован новый гальванографический метод, позволивший выявить динамическую составляющую скорости растворения пассивного металла, характеризующую количество и анодную активность дефектных мест пассивирующей пленки. [9]
Скорость растворения металла в области устойчивой пассивности определяют весовым, аналитическим методом. [10]
У легированных чугунов появляется область устойчивой пассивности. [11]
На диаграмме отмечается также область неполной пассивности. [12]
При выдержке стали в области устойчивой пассивности плотности тока снижаются до 1 10 - 3 А / м2 ( см. табл. 3.1), что соответствует скорости растворения 0 002 мм / год. Перемешивание и повышение температуры до 40 С в 25 % - ном растворе мало влияют на скорость растворения стали в пассивном состоянии в отличие от растворов углеаммиакатов, содержащих аммиачную селитру. В разбавленных чистых 2 5 - 5 % - ных растворах аммиака при рН 11 7 - 11 9 ( рис. 3.2 кривая 1), контактирующих с воздухом, углеродистая сталь находится в устойчивом пассивном состоянии. После выключения катодной поляризации стационарный потенциал стали увеличивается до величины, большей - 0 5 В, а на анодной поляризационной кривой фиксируется лишь область пассивного состояния и перепассивации. [13]
 |
Поляризационные кривые в водном растворе, насыщенном сероводородом, для алюминиевого покрытия. [14] |
В присутствии ионов хлора области пассивности для алюминиевых покрытий при всех плотностях тока отсутствуют. Однако степень анодного и катодного контроля достаточна для обеспечения высокой коррозионной стойкости. [15]
Страницы: 1 2 3 4
