Область - пассивность
Cтраница 2
 |
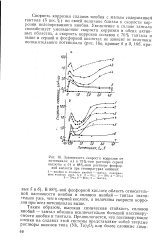
Поляризационные кривые в водном растворе, насыщенном сероводородом, для алюминиевого покрытия. [16] |
В присутствии ионов хлора области пассивности для алюминиевых покрытий при всех плотностях тока отсутствуют. [17]
 |
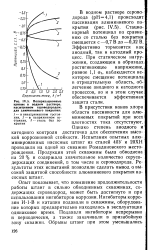
Коррозия хромистых сталей в растворах H2SO4 при 50. а - Х27 ( 1. б - в увеличенном масштабе для сталей, дополнительно легированных 3 % Pt ( 2 или 3 % Pd ( 3. [18] |
Роха [148] по расширению области пассивности при контактировании с платиной стали Х27, легированной небольшими количествами Mo, Ni, Си. Хром, являющийся важным компонентом нержавеющих сталей, легко пассивируется. [19]
При дальнейшем повышении потенциала за область вторичной пассивности плотность анодного тока возрастает и происходит растворение никеля через окисную пленку ( в основном в виде № 3), сопровождаемое выделением кислорода. Коррозионное поведение никеля в кислых растворах в областях перепассивации, вторичной пассивации и далее представляет ограниченный практический интерес, так как эти потенциалы выходят за пределы изменения окислительно-восстановительных потенциалов большинства водных растворов. [20]
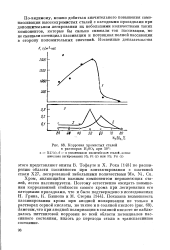
Если в растворе присутствует хлор-ион, область пассивности сокращается, и тем в большей степени, чем выше-концентрация хлор-иона. При достаточно большой концентрации хлор-иона электродный ] потенциал сплава АМгб лежит уже в области потенциала пробоя. [21]
На анодных характеристиках хромистых чугунов отсутствует область пассивности и потенциал коррозии расположен в области потенциалов анодного активирования. С увеличением содержания хрома ветвь анодного активирования смещается в направлении положительных значений потенциала. [22]
Металл конструкции или сооружения должен иметь область пассивности с достаточно низкой скоростью растворения, к-рая лимитируется не только разрушением металла, но и возможным загрязнением среды. Широко применяют анодную защиту для оборудования, работающего в серной к-те, средах на ее основе, водных р-рах аммиака и минер, удобрений, фосфорной к-те, в целлюлозно-бумажной пром-сти и раде отд. Особенно важна анодная защита теплообменного оборудования из легир. Регулирование потенциала металла осуществляют автоматич. Зона действия защитных потенциалов зависит от области оптим. В ( титановые сплавы) до неск. [23]
Участок ВС отвечает области пассивации или области неустойчивой пассивности. В этой области с ростом потенциала скорость растворения уменьшается. [24]
Для поддержания зоны защитных потенциалов в области устойчивой пассивности использован единичный контур регулирования и контроля потенциала ( рис. 8.23) унифицированной автоматической системы анодной защиты Донец-12 [5], позволяющий поддерживать потенциал в заданном режиме. [25]
Поляризация от внешнего источника также способна изменять область пассивности. Катодная поляризация может переместить потенциал из пассивной области в активную ( см. рис. 1.11), поэтому необходимо принимать меры к тому, чтобы не допускать контактов с любым другим корродирующим металлом. [27]
Следует также учесть, что и в области пассивности может идти коррозия железа с конечной, пусть даже относительно небольшой скоростью, которая определяется растворимостью пассивирующего защитного слоя. [28]
Здесь между линиями / и 2 расположена область гидридной пассивности. Ионы Ti2 при обычной температуре могут окисляться водой [27] или растворенным в ней кислородом, а при Ф - 0 37 В - электрохимически. [29]
Страницы: 1 2 3 4