Область - кислый раствор
Cтраница 2
Эти области ограничены кривой N M - MN растворимости кристаллогидратов в кислых растворах и линиями перехода кристаллогидратов. Ниже и левее линии растворимости находится область ненасыщенных кислых растворов. [16]
Скорость разряда водорода на амальгаме натрия не зависит от рН раствора, поэтому сведения о трудности выделения водорода на амальгамном электроде вследствие подщелачивания прика-тодного слоя несостоятельны. Возрастание величины рН может влиять на кинетику выделения водорода только в области кислых растворов. [17]
Из рассмотрения этой кривой ясно, что она совершенно подобна кривым титрования растворов слабых оснований сильными кислотами. Действительно: а) как и при титровании слабых оснований, точка эквивалентности лежит здесь в области кислых растворов ( при рН5 0); около точки эквивалентности имеется скачок рН ( от рН6 до рН4), допускающий точное титрование; б) в соответствии со сказанным, рассматриваемую соль ( как и слабые основания) можно титровать с индикаторами метиловым оранжевым и метиловым красным, но нельзя титровать с фенолфталеином. [18]
Из рассмотрения этой кривой ясно, что она совершенно подобна кривым титрования растворов слабых оснований сильными кислотами. Действительно: а) как и при титровании слабых оснований, точка эквивалентности лежит здесь в области кислых растворов ( при рН 5 0); около точки эквивалентности имеется скачок рН ( от рН 6 до рН 4), допускающий точное титрование; б) в соответствии со сказанным, рассматриваемую соль ( как и слабые основания) можно титровать с индикаторами метиловым оранже вым и метиловым красным, но нельзя титровать с фенолфталеином. [19]
Из рассмотрения этой кривой ясно, что она совершенно подобна кривым титрования растворов слабых оснований сильными кислотами. Действительно: а) как и при титровании слабых оснований, точка эквивалентности лежит здесь в области кислых растворов ( при рН 5 0); около точки эквивалентности имеется скачок рН ( от рН б до рН 4), допускающий точное титрование; б) в соответствии ср сказанным, рассматриваемую соль ( как и слабые основания) можно титровать с индикаторами метиловым оранжевым и метиловым красным, но нельзя титровать с фенолфталеином. [20]
Области существования этих кристаллогидратов находятся в пределах заштрихованных криволинейных треугольников: в треугольнике S M - тетрагидрат, в треугольнике S MMi - тригидрат, в треугольнике S2NM - дигидрат. Эти области ограничены кривой N M MN растворимости кристаллогидратов в кислых растворах и линиями перехода кристаллогидратов. Ниже и левее линии растворимости находится область ненасыщенных кислых растворов. [21]
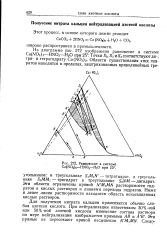 |
Равновесие в системе Ca ( N03 2 - HN03 - H2O при 25. [22] |
Эти области ограничены кривой N M MN растворимости гидратов в кислых растворах и линиями перехода гидратов. Ниже и левее линии растворимости находится область ненасыщенных кислых растворов. [23]
На диаграмме рис. 108 изображено равновесие в системе Ca ( NO3) 2 - HNO3 - Н2О при 25 С. Области существования этих кристаллогидратов находятся в пределах заштрихованных криволинейных треугольников: в треугольнике StMiN - тетрагидрат, в треугольнике S3MMi - тригидрат, в треугольнике S2MN - дигидрат. Эти области ограничены кривой N M MN растворимости кристаллогидратов в кислых растворах и линиями перехода кристаллогидратов. Ниже и левее линии растворимости находится область ненасыщенных кислых растворов. [24]
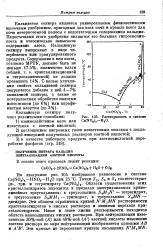 |
Растворимость в системе Ca ( N08 2 - H20. [25] |
На диаграмме рис. 104 изображено равновесие в системе Ca ( N08) z - HN03 - H20 при 25 С. Области существования этих кристаллогидратов находятся в пределах заштрихованных криволинейных треугольников: в треугольнике S M N - тетрагидрат, в треугольнике 83ММг - тригидрат, в треугольнике StMN - дигидрат. Эти области ограничены кривой N M MN растворимости кристаллогидратов в кислых растворах и линиями перехода кристаллогидратов. Ниже и левее линии растворимости находится область ненасыщенных кислых растворов. [26]
Страницы: 1 2