Область - метастабильное состояние
Cтраница 3
Во-первых, в данном случае необходимо учитывать видоизменение характера хлопьеобразования гидроксида алюминия под воздействием магнитного поля. Доказано, что магнитное поле оказывает влияние на процесс образования в растворе новой фазы. Наложение магнитного поля видоизменяет прежде всего процессы, происходящие в области метастабильного состояния раствора, приводит к изменению характера зародышеобразования частиц новой фазы и, как следствие, изменению модификации образующейся структуры дисперсной фазы. В рассматриваемом случае действие магнитного поля может сказаться на процессе зародышеобразования мельчайших кристалликов гидроксида алюминия при пересыщении воды этим малорастворимым компонентом, образующимся в ходе электрохимического растворения анода. [31]
Существование спинодали приводит к тому, что изобара может пересечь изотерму в двух точках, соответствующих различным значениям объема. Это означает возможность равновесия двух фаз с различными объемами - фазовое равновесие первого рода. На бинодали коэффициенты устойчивости не равны нулю; между бинодалью и спинодалью существуют области метастабильных состояний системы, в которых каждая из фаз может существовать только при отсутствии другой фазы. [32]
Существование спинодали приводит к тому, что изобара может пересечь изотерму в двух точках, соответствующих различным значениям объема. Это означает возможность равновесия двух фаз с различными объемами - фазового равновесия первого рода. На бинодали коэффициенты устойчивости не равны нулю; между бинодалью и спинодалью существуют области метастабильных состояний системы, в которых каждая из фаз может существовать только при отсутствии другой фазы. [33]
На этом рисунке по оси абсцисс отложено значение разведения раствора для того, чтобы показать, что полученные изо-стрессы вязкости ( линии равного напряжения сдвига) внешне похожи на изотермы реального газа. Действительно, разведение характеризует объем, занимаемый макромолекулами, а вязкость раствора характеризует взаимодействие между макромолекулами так же, как давление в газе отражает взаимодействие его молекул. Из рисунка видно, что при работе с растворами можно получить всю кривую, включая область метастабильных состояний, что невозможно сделать при переходе газ - жидкость. [34]
При этой температуре уровень стабильности системы не изменяется при плавлении, и поэтому такое плавление называю плавлением с нулевым производством энтропии ( разд. При дальнейшем нагревании выше равновесной температуры плавления метастабильный расплав становится стабильным. Поскольку характеристики равновесного плавления можно определить, а затем экстраполировать с достаточной точностью их значения в область метастабильного состояния, возможно также, исходя из температуры плавления с нулевым производством энтропии, установить уровень стабильности исходного кристалла. На рис. 9.2 приведены результаты такого расчета для полиэтилена, закристаллизованного из расплава. Из рисунка видно, что в образце нет очень совершенных кристаллов. Резкий подъем кривой распределения кристаллов в - области более низких значений свободной энтальпии может быть обусловлен складыванием полимерных цепей. [35]
Там компонент В кристаллизуется из расплавов качественно одного и того же состава как вдоль кривой bd, так и вдоль кривой се. Температура кристаллизации является функцией концентрации А или В как для одного отрезка, так и для другого. Следовательно, оба отрезка являются ветвями одной и той же кривой и могут быть соединены друг с другом отрезком cd, характеризующим область метастабильных состояний. [36]
Многие высокомолекулярные соединения могут давать одну или несколько кристаллических фаз. Способность кристаллизоваться для природных белковых веществ установлена довольно давно; несколько позднее были получены кристаллы синтетических полимеров. Диаграммы состояний, описывающие равновесие в простейших системах кристаллизующийся полимер - растворитель, сходны с диаграммами состояний низкомолекулярных кристаллизующихся веществ. Растворы, попадающие в области метастабильных состояний, самопроизвольно разделяются на две фазы: одной из них является раствор полимера, а другой - кристаллический полимер ( иногда содержащий некоторое количество растворителя) или кристаллический растворитель. Мета-стабильные растворы, концентрация которых отвечает эвтектической точке, полностью отвердевают, образуя эвтектику - высокодисперсную смесь кристаллов полимера и растворителя. Выше так называемой линии ликвидуса устойчивы жидкие фазы; это - область существования стабильных гомогенных растворов полимера. [37]
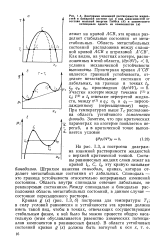 |
Диаграмма взаимной растворимости жидкостей в бинарной системе ( а и вид зависимостей от состава мольной энергии Гиббса ( б и химического потенциала одного из компонентов ( в. [38] |
Штрихом нанесена спинодаль, кривая, которая отделяет метастабильные состояния от лабильных. Область внутри спинодали отвечает лабильным, не реализуемым состояниям. Между спинодалью и бинодалью расположена область метастабильных состояний, в данном случае - состояние пересыщенного раствора. [39]
 |
Кривая испарения ( давления насыщенного пара. [40] |
Все кривые давления пара имеют одинаковую общую форму, подобную приведенной на рис. 2 - 2, причем кривая своей выпуклостью обращена к оси температур на Р, Г - диаграмме. Верхней границей кривой испарения является критическая точка. При этой температуре система становится гомогенной и никакое давление не вызовет образования жидкой фазы. Нижняя граница кривой испарения определяется областью метастабильного состояния переохлажденной жидкости. [41]
Если такие кривые построить для различных температур, то геометрическим местом точек А и В является кривая / на рис. 11.7 6, называемая бинодалью. Это кривая взаимного смешения, подробно рассмотренная в гл. Геометрическим местом точек М и N является кривая 2 на рис. 11.7 6, называемая спино-далью. Бинодаль отделяет область устойчивых состояний от метастабильных, каждая ее точка отвечает неравенству cPg / dx t 0; спинодаль отделяет область метастабильных состояний от неустойчивых. [42]
Следует иметь в виду, что в зоне контакта горячего, почти насыщенного питающего раствора с гораздо более холодным, слабо пересыщенным маточным раствором температура питающего раствора резко понижается и если граница метастабиль-ного состояния раствора расположена вблизи кривой растворимости, то при смешении может произойти самопроизвольное образование зародышей. Поэтому соотношение питающего и циркулирующего маточного растворов тщательно контролируется. При расчете кристаллизатора учитывается, что смешение обоих растворов должно быть полным и происходить мгновенно. Соотношение между двумя потоками регулируется таким образом, чтобы раствор после смешения при конечной температуре был либо ненасыщенным ( тогда в нем растворяются все вновь образующиеся зародыши), либо насыщенным, либо слабо пересыщенным, но находился при этом в области устойчивого метастабильного состояния. [43]
Графически это равновесие изображается кривой зависи-юсти давления насыщенного пара от температуры. Давлением насыщенного пара называется равновесное давление, которое создается ри Т const некоторым количеством вещества в закрытом сосуде, е содержащем посторонних газов. Кривая снизу граничена областью метастабильного состояния переохлажденной шдкости, а сверху - критической точкой. [44]
Графически это равновесие изображается кривой зависимости давления насыщенного пара от температуры. Давлением насыщенного пара называется равновесное давление, которое создается при Т const некоторым количеством вещества в закрытом сосуде, не содержащем посторонних газов. Кривая снизу - ограничена областью метастабильного состояния переохлажденной жидкости, а сверху - критической точкой. [45]
Страницы: 1 2 3 4