Облучение - крыса
Cтраница 1
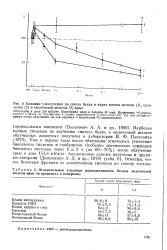
Облучение крыс ( более 20 мВт / см2, более 14 мВт / г, не менее 18 Дж / г) ЭМ-полем ( 0 6 - 0 9 ГГц) вызывает аналогичную реакцию ( Лин и др., 1977, д Андреа и др., 1977, цит. Следует заметить, что частота поля 0 6 - 0 9 ГГц для крыс является резонансной. При поглощенной дозе облучения более 20 Дж / r нарушается физическая выносливость крыс. [1]
После облучения крыс тепловыми нейтронами от ядерного реактора количество кофермента-I в печени временно понижалось. [2]
На 21 - 31 - е сутки после облучения крыс в дозе 600 р сперматогенез почти полностью отсутствует. Признаки начинающегося восстановления обычно появляются к концу первого месяца после воздействия. Клетки Сертоли и эпителий придатка яичка изменяются незначительно. У морских свинок облучение в дозе П5р вызывает раннюю гибель сперматогоний и небольшого количества сперматоцитов с последующим фактическим прекращением всего сперматогенеза. [3]
Голубенцевым ( 1961) уменьшение количества макроэргических соединений в селезенке через 3 ч после облучения крыс в дозе 193 5 мКл / кг также обусловлено истощением фонда АТФ. [4]
Отмечено также повышение содержания цАМФ в печени в период 24 - 48 ч после облучения крыс в дозе 387 0 - 645 0 мКл / кг. [5]
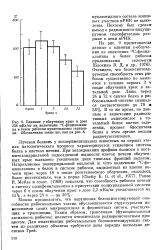 |
Влияние v-облучения крыс в дозе 258 мКл / кг на включение 14С - фенилалани-на в белок рибосом нуклеоплазмы селезенки. Обозначения такие же, как на 8. [6] |
Очевидно, что белоксинтези-рующая способность этих рибосом существенно не меняется в течение первых 3 ч посде облучения крыс в летальной дозе. В то же время, по данным о включении радиоактивных аминокислот в тотальный белок клеток селезенки, процесс биосинтеза белка в этом органе весьма радиочувствителен. [7]
 |
Кривые выживаемости кроликов после тотального облучения в дозе 10 Гр. [8] |
Сравнение защитной дозы цистамина ( 50 мг / кг), вводимой внутрибрюшинно за 10 мин до облучения крыс, и пероральной дозы 600 мг / кг, вводимой зондом за 30 мин до облучения, показало, что они дают аналогичный защитный эффект, однако пероральная доза ( 600 мг / кг) достигает уже пороговой летальной дозы. [9]
В дальнейших исследованиях, проведенных с помощью ультрацентрифугирования клеток в градиенте плотности альбумина, было показано, что - облучение крыс в дозе 154 8 мКл / кг снижает активность аспартат - карбамоилтрансферазы тех фракций клеток костного мозга и селезенки крыс, которые в норме характеризуются повышенной активностью этого фермента. Отмечено, что облучение способствует диссоциации регуляторных субъединиц, ингиби-рующих каталитические центры в молекуле аспартат - карбамоилтрансферазы. Присутствие ЦТФ снижает степень угнетения фермента, индуцируемого облучением, но подавляет функциональную активность изолированных каталитических субъединиц молекулы облученного фермента. Bigler и В. М. Tolbert, свидетельствуют о том, что при облучении животных в дозах, близких к летальным, изменение активности этого фермента в тканях не может быть обусловлено прямым или непрямым действием ионизирующих излучений на его молекулы. [10]
ДНК-синтезирующих ферментов увеличивается в несколько раз. Облучение крыс в ранние сроки после частичной гепатэктомии, когда осуществляется синтез этих ферментов, наиболее губительно для регенерирующего органа. Через 6 ч после операции облучение крыс ведет к сильному ингибированию ДНК-поли-меразной и тимидинкиназной активности [ Chambon P. Изучая репарацию однотяжевой ДНК в клетках печени, селезенки, ви-лочковой железы и лимфатических узлов крыс после облучения к дозах 232 - 3870 мКл / кг, Б. П. Иванников и соавт. ДНК клеток млекопитающих зависит от интенсивности белкового синтеза. [11]
Для оценки возможной роли катаболизма в постлучевой гипоаль-буминемии были проведены специальные исследования с использованием меченных тритием белков сыворотки крови [ Renter A. Установлено, что скорость распада альбуминов и - глобулинов после облучения крыс в дозе 206 4 мКл / кг увеличивается. [12]
Терещенко [20] разработал новый метод определения дезоксицитидина в моче крыс, обеспечивающий высокую степень очистки выделяемого нуклеозида. Этот метод показал, что экскреция дезоксицитидина в первые сутки после облучения крыс ( 800 р) очень сильно возрастает - в 20 раз и более. [13]
Изменения постоянных концентраций циклических нуклеотидов в печени в динамике лучевой болезни не могут не отражаться на многих биохимических процессах в этой ткани. Обнаруженное угнетение фосфорилирования гистона HI в печени через 2; 12 и 24 ч после облучения крыс в дозе 206 4 мКл / кг [ Цудзевич Б. А. и др., 1980 ] не связано, по-видимому, с уровнем цАМФ, неизменяющимся в эти сроки. Дело в том, что гистон HI фосфорилируется цАМФ - зависимой гистонкиназой 1 в N-концевой трети молекулы в положении серин-37. Независимая от циклических нуклеотидов гис-тонкиназа 2 катализирует фосфорилирование в центре молекулы гистона в положении серин-106 [ Malette L. Возможны и другие объяснения. Например, может происходить активация белкового ингибитора киназ зши усиление процессов дефосфорилирования с помощью фосфопро-теинфосфатаз. [14]
Страницы: 1 2