Обмен - катион
Cтраница 2
Процесс обмена катионов рассматривается в настоящее время как обратимая гетерогенная химическая реакция, протекающая на поверхности твердой фазы катионита. [16]
Скорость обмена катионов зависит от их диффузии к поверхности раздела катионит-вода и определяется структурой катионита. При компактной структуре катионита обмен происходит быстро и в основном на наружных поверхностях - экстрами-целлярный обмен. Однако при этом не полностью используется сорбционная емкость катионита. [17]
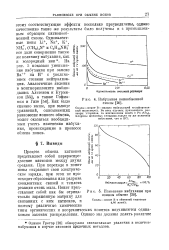 |
Набухание ионообменной смолы.| Изменение набухания при ионном обмене. [18] |
Процесс обмена катионов представляет собой перераспределение катионов между двумя средами. При переходе в ионит ионы сохраняют свои электрические заряды, при этом не происходит образования или разрыва ковалентных связей и теплота реакции очень мала. Ионит представляет собой как бы отрицательно заряженную матрицу для связанных с ним катионов, и поэтому различные химические типы органических и неорганических нонитов подчиняются одинаковым законам распределения. [19]
Эквивалентность обмена катионов, неизменность концентрации анионов в исходном и равновесном растворах, а также то обстоятельство, что морфин из эспатита, в особенности при малой степени использования емкости, не может быть извлечен без вытесняющего иона, подтверждают ионообменный механизм адсорбции. [20]
Скорость обмена катионов зависит от их диффузии к поверхности раздела катионит - вода и определяется структурой катионита. При компактной структуре катионита обмен происходит быстро и в основном на наружных поверхностях - экстрамицеллярный обмен. Однако, при этом не полностью используется сорбционная емкость катионита. [21]
Исследованию обмена катионов на минеральных и синтетических ионитах в зависимости от температуры уделено крайне малое внимание. [22]
Реакция обмена катионов обратима. После поглощения какого-либо катиона из раствора ( например, К) и вытеснения из почвы другого катиона ( например, Са) поглотившийся катион может быть снова вытеснен в раствор. [23]
Степень обмена катионов Na на катионы Са2, равная 18 - 20 %, стабилизирует цеолитный катализатор. Дальнейшее увеличение степени обмена на катионы Са2 не улучшает каталитические свойства. [24]
При этом обмен катионов совершается в строго эквивалентных ( равнозначных) количествах. [25]
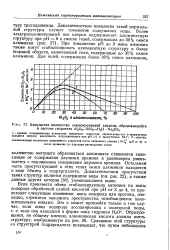 |
Кажущееся количество алюмокремневой кислоты, образовавшейся в системе гидрогеля А12Оз - 5Ю2 - Н2О - Na2SO4. [26] |
Если произвести обмен стабилизирующих катионов на ионы водорода обработкой слабой кислотой при рН от 3 до 4, то происходят следующие изменения: ионы водорода или протоны, очевидно, стремятся заполнить пространство, освобожденное положительными ионами. [27]
Основы теории обмена катионов заложены исследованиями советских ученых, среди которых в первую очередь следует упомянуть академика К. К. Гедройца [1], создавшего стройное учение об обмене ионов в почвах. Общие положения ионного обмена, установленные К. К. Гед-ройцем на почвах, получили дальнейшее развитие в работах Б. П. Никольского [2-10], Е. Н. Гапона [11, 12] и других, создавших количественную теорию ионообменных процессов. Эта теория была проверена на алюмосиликатах и затем с успехом перенесена па другие катионные поглотители. [28]
Рассмотрим процесс обмена катионов 1 и 2 внутри частицы ионита. [29]
В результате обмена катионов растения поглощают освободившиеся катионы, а почва закисляется. Поэтому при закислении почв возможно и повышение концентраций растворимых форм А1 и Fe. При оценке влияния кислотных дождей на водоемы необходимо учитывать не только возможные реакции, протекающие в почве, но и длительность контакта с почвокорневой системой. [30]
Страницы: 1 2 3 4