Обмен - водород
Cтраница 2
Скорость обмена водорода на тритий у атома Cg пурино-вого кольца в полиадениловой кислоте зависит от распределения электронной плотности в пурине. Это распределение изменяется при конформационных движениях, вызванных сдвигом рН и комплексообразованием с полиуридиловой кислотой. Скорость изотопного обмена весьма чувствительна к таким изменениям электронной плотности. [16]
Реакция обмена водорода, присоединенного к бору в N-замещенных боразинах, в других отношениях детально не была исследована. Так как В-тригало-генборазины - намного более легко доступные соединения, их используют главным образом для последующих реакций обмена, поэтому отсутствие попыток осуществить обмен связанного с бором водорода вполне понятно. [17]
Реакция обмена водорода с дейтерием между 140 и 491 К: Н2 - f - D2 2HD, которая подробнее будет описана в следующей главе, при более высоких температурах происходит с преобладанием хемосорбции водорода. При низких температурах Смит и Тэйлор [54] обнаружили преимущественно физическую адсорбцию дейтерия. [18]
Изучение обмена водорода в связях Р - Н на дейтерий тяжелой воды обнаруживает отсутствие таутомерии в анионе фос-форноватистой кислоты, в фосфористой кислоте и ее анионе и подтверждает ее существование в недиссоциированной фосфор-новатистой кислоте. [19]
Факт обмена водорода в насыщенных углеводородах1 можно истолковать как следствие поляризации а-связи исключительно энергично действующими электронодонорными и электроноакцепторнымн реагентами. При этом разветвление углеродной цепи, вероятно, должно сказываться противоположным образом. [20]
Исследованию обмена водорода между органическими соединениями и окисью дейтерия DoO, тяжелым этиловым спиртом C2HsOD, тяжелым аммиаком ND3 и тяжелыми кислотами посвящено много сотен сабот. Все имеющиеся в литературе данные по этому вопросу собраны и табл. 14, 15 и 17, а важнейшие выводы из опытного материала, теоретические представления и обобщения рассмотрены ниже. [21]
Отсутствие обмена водорода на дейтерий для солей диазония ArN2 в среде D2O исключает образование дегидробензола в качестве ингермедиата. Малая селективность по отношению к различным нуклеофилам в конкурирующих реакциях свидетельствует о высокой активности ингермедиата и согласуется с образованием арил-катиона в качестве такого ингермедиата. [22]
Скорость обмена водорода в определенной связи ароматического соединения удобно выражать отношением к скорости обмена водорода в бензоле в тех же условиях. [23]
Относительные скорости обмена водорода в полициклических ароматических углеводородах ( табл. 40) хорошо объясняются с помощью электростатической модели эффекта поля [15, 42], поскольку наблюдается хорошая линейная корреляция между логарифмами относительных констант скоростей обмена и суммой обратных величин расстояний между атомами углерода, несущими отрицательный заряд, и каждыми другими я-углеродными атомами в молекуле. [24]
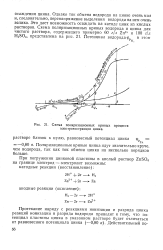 |
Схема поляризационных кривых процесса электроэкстракции цинка. [25] |
Однако ток обмена водорода на цинке очень мал и, следовательно, перенапряжение выделения водорода на нем очень велико. Это дает возможность осаждать на катоде цинк из кислых растворов. [26]
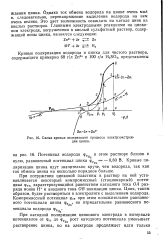 |
Схема кривых поляризации процесса электроэкстракции цинка. [27] |
Однако ток обмена водорода На цинке очень мал и, следовательно, перенапряжение выделения водорода на нем очень велико. Это дает возможность осаждать на катоде цинк из кислых растворов. [28]
При рассмотрении обмена водорода в С - Н - связях органических веществ в любых средах в первую очередь необходимо учитывать химическую природу реагента, вызывающего изотопную реакцию. От нее зависит проявление разных сторон реакционной способности органических веществ, которая нас интересует, когда мы изучаем реакции изотопного обмена водорода. При этих реакциях имеют значение кислотно-основные свойства органического вещества, которые определяются его строением, но обусловлены также химической природой атакующего реагента и особенностями реакционной среды. [29]
При реакции обмена водорода на дейтерий эти же окислы металлов на носителе, восстановленные при 500, становятся более активными. Так, данные табл. 6 указывают на увеличение скорости реакции каталитического обмена водород - дейтерий на окисных катализаторах после восстановления их водородом. [30]
Страницы: 1 2 3 4