Обмен - водород
Cтраница 3
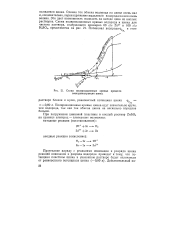 |
Схема поляризационных кривых процесса электроэкстракции цинка. [31] |
Однако ток обмена водорода на цинке очень мал и, следовательно, перенапряжение выделения водорода на нем очень велико. Это дает возможность осаждать на катоде цинк из кислых растворов. [32]
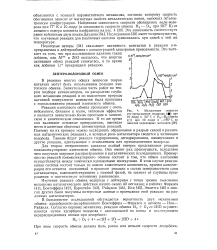 |
Абсолютные скорости о-я-превращения водорода ( при 10 торр и 26 С и Н3 - О2 - обмена ( О при 10 торр и - 196 С на окислах переходных металлов. [33] |
Изучение реакции обмена водорода с дейтерием с точки зрения выяснения механизма каталитического действия начато около 40 лет назад; в работах Фаркаса [41], Бонгоффера [42], Бурштейн [43], Райдила [44], Или [45], Эмметта [46] и многих других были получены интересные данные о протекании этой реакции на различных катализаторах. [34]
Гораздо труднее протекает обмен водорода в связях С - Н органических соединений. Лишь у небольшого числа пеществ обменивается водород связей C - ti с подои и спиртом. [35]
Величина константы скорости обмена водорода в толуоле сильно зависит от кислотности среды. [36]
Последовательность констант скорости обмена водорода в диметиланилине и трифениламине с трифторуксусной кислотой противоположна той последовательности, которая установлена для дейтерообмена с уксусной кислотой. Замедление водородного обмена в диметиланилине при усилении кислоты и повышении диэлектрической постоянной зависит от увеличения энергии активации обменной реакции. [37]
Что касается стереохимии обмена водорода в амбидентных системах, то еще в 1936 г. Уилсоном и Ингольдом [52, 53] было установлено, что скорости D-обмена и рацемизации оптически активного 2-бензоилбутана в системе диоксан - D20 / NaOD равны. Это было объяснено предположением, что реакция протекает через стадию отрыва протона, приводящую к образованию плоского енолят-иона. Захват протона амбидентным ионом происходит быстрее по атому кислорода, чем по атому углерода. [38]
Активность в реакции обмена водорода на дейтерий наблюдается только для катализаторов, имеющих как электронодонорные, так и электроно-акцепторные свойства и практически отсутствует у алюмосиликатов, которые обладают незначительной восстановительной силой. Тем не менее, полученные данные содержат мало доказательств в пользу того, что окислительно-восстановительная активность является решающим фактором для процесса обмена, поскольку активность в передаче электрона у окиси алюминия все еще быстро возрастает для температур активации 550 - 650 С, тогда как активность в реакции обмена быстро уменьшается. [39]
Ацилированием называется реакция обмена водорода аминогруппы, оксигруппы или ароматического кольца на ацильную группу ( ацил) - остаток карбоновой или кислородсодержащей минеральной кислоты. [40]
С изобутаном скорость обмена первичного водорода возрастает в 35 раз при переходе от 91.5 % - ной кислоты к 98 3 % - ной. Прибавление следов изобутилена влечет за собой сильное возрастание скорости обмена. [41]
 |
Изотопный эффект в теплоемкости этилендейтерогликоля. [42] |
Образец D-ПВС получен путем двукратного обмена водорода между Н - ПВС и тяжелой водой и высушен в вакууме над пятиокисью фосфора. Содержание дейтерия в гидроксильных группах определено по отношению интенсивностей полос валентных колебаний О-D и О - Н в инфракрасном спектре и составляло 92 ат. [43]
Известно, что ток обмена водорода и скорость изотопного обмена на палладиевом электроде очень велики. Палладиевый электрод функционирует как обратимый водородный. Если бы в промежуточной стадии каталитического разложения наблюдалось образование адсорбированного атомарного водорода, то он быстро обменивался бы с водородом в растворе и мы не наблюдали бы никакого обогащения изотопного состава выделяющегося водорода. [44]
Пиридин вступает в реакцию обмена водорода с гораздо большей скоростью, чем бензол. Это объясняется наличием в кольце электроотрицательного атома азота. По кинетической СН-кислотности пиридин похож на фторбеизол, однако между ними имеется одно важное различие. В молекуле фторбеизола более кислой является ближайшая к атому фтора связь СН в положении 2 и кислотность уменьшается в последовательности 2 - СН3 - СН4 - СН. [45]
Страницы: 1 2 3 4