Контактный обмен
Cтраница 3
Но означает ли все изложенное, что гипотеза контактного обмена верна. [31]
Предполагается [13], что действие ПАВ в процессе контактного обмена наиболее эффективно, когда они тормозят катодный и анодный процессы одновременно. Добавки, тормозящие только анодный процесс, можно вводить и в электролит меднения, и з слабый раствор серной кислоты предварительного активирования стали перед меднением. [32]
Металлы замедленного разряда 313 ионизации 257 квазиравновесные 269 контактного обмена 153 методы исследования 404 ел. [33]
Такой обмен эти авторы назвали контактным, В принципе контактный обмен возможен только между мицеллами одного знака заряда. Если речь идет о катионах, то они могут, по гипотезе этих авторов, перескакийать с отрицательно заряженной коллоидной частицы почвы на имеющую тот же знак заряда поверхность корневого волоскд и обратно. [34]
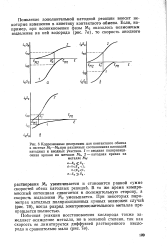
Появление дополнительной катодной реакции вносит некоторые изменения в кинетику контактного обмена. [36]
Движение электролита: в зависимости от характера контроля процесса контактного обмена оказывает различное воздействие. Зависимость между скоростью цементации ( и) и угловой скоростью вращения диска ( со) описывается в этом случае [96] уравнением Левина. [37]
Добавление к электролиту фосфорнокислых солей аммония способствует уменьшению скорости контактного обмена ( вытеснению меди железом), что улучшает сцепление медного покрытия со сталью. [38]
Процесс химической металлизации, в отличие от процессов коррозии и контактного обмена, характеризуется основными реакциями восстановления ионов металла, находящихся в растворе, и окислением восстановителя, также присутствующего в растворе, на каталитически активной поверхности электрода. Здесь окислитель и восстановитель находятся в растворе, не взаимодействуя друг с другом, и для протекания реакции необходим катализатор. Например, по отношению к реакции химического никелирования каталитически активными металлами являются палладий, никель, железо, кобальт. [39]
При погружении железа в раствор, содержащий Bi3, происходит реакция контактного обмена, вызванная тем, что стандартные потенциалы электродов Fe2 Fe и Bi3 Bi соответственно равны - 0 4402 и 4 - 0 2150 В. [40]
Проводится предварительная пассивация поверхности покрываемых изделий [25, 26], что уменьшает интенсивность контактного обмена в отсутствие внешнего тока. В процессе электролиза пленка частично восстанавливается [149, 151, 152] и возникает большое число активных участков, что - приводит к равномерному распределению осадка, увеличению площади сцепления основного металла с покрытием и снижению пористости осадка. [41]
Если восстанавливающийся металл полностью закроет поры осадка ( SK-1), то контактный обмен прекращается и потенциал электрода ( компромиссный потенциал) принимает значение, соответствующее равновесному потенциалу электроположительного компонента в данном растворе. Действительно, если скорость цементации контролируется отводом ионов растворяющегося металла, то толщина и пористость осадка непосредственно влияют на скорость процесса. [42]
С целью интенсификации процесса меднения при комнатной температуре и большего подавления реакции контактного обмена при осаждении покрытий на сталь в дифосфатный электролит вводили [56] комплекс органических красителей при следующем соотношении компонентов ( г / л): 80 - 90 CuSO4 - 5H2O, 350 - 380 К4Р2О7, 20 - 30 трилона Б, 0 021 - 0 023 азокрасителя кислотного желтого, 0 021 - 0 023 трифенилметанового красителя ура-нина А, 0 1 - 0 3 мл / л смачивателя Прогресс, рН 8 0, i 0 8 - 2 0 А / дм2, перемешивание электролита. Получаемые покрытия характеризуются совершенством текстуры. [43]
Аналогия между цементацией и коррозией позволяет использовать коррозионные диаграммы для оценки некоторых параметров контактного обмена. Расчетные формулы были получены Антроповым [22, 46, 62, 104, 121] на основе следующих соображений. [44]
Дана О бщая характеристика процесса цементации; рассмотрены условия его протекания, роль контактного обмена, влияние состава раствора и других факторов на скорость протекания процесса. [45]
Страницы: 1 2 3 4