Образец - окись - алюминий
Cтраница 1
Образцы окиси алюминия, вакуумированные при температурах выше 650, как показано на этом же рисунке, имеют три основные полосы поглощения. Интересные результаты были получены Базилой ( 1962) для алюмосиликата, в спектре которого была найдена только одна узкая полоса поглощения при 3750 см 1, возможно имеющая плечо с низкочастотной стороны. [1]
Образцы окиси алюминия, приготовленные из алюмината натрия и содержащие около 0 1 % ионов натрия, имели большое число слабых кислотных центров и поэтому оказались прекрасными дегидратирующими катализаторами. В то же время эти образцы окиси алюминия не изомеризовали циклогексен из-за отсутствия сильных кислотных центров, которые были нейтрализованы ионами щелочного металла. Пайнс и Хааг [36] определили, что верхний предел общего числа кислотных центров, способных дегидратировать бута-нол, и верхний предел числа сильных кислотных центров, способных изомеризовать циклогексен, составляли 10 - Ю12 и 8 - Ю12 центров на 1 см2 соответственно. [2]
Образцы окиси алюминия АК и АН были приготовлены гидролизом изопропилата алюминия. [3]
Образцы окиси алюминия марок Алкоа F - l, F-10 и Харшоу 0104 обычно пригодны после активации при 110 С. В условиях высоких температур на образцах Алкоа F-1 и Харшоу 0104 ( Н-0104) происходит полимеризация изобутилена, следовательно, они не могут быть использованы. Образец F-1 выдерживал более высокую температуру активации, прежде чем на нем обнаруживали полимеризацию изобутилена. Однако на этом образце наблюдается увеличение удерживаемых объемов по сравнению с образцами F-10 и Н-0104, а также удлиняется продолжительность анализа без улучшения разделения. Поэтому применение образца F-1 нежелательно. [4]
Если образцы окиси алюминия не подвергаются высокотемпературной дегидратации, приводящей к сс-окиси, то они содержат от нескольких десятых до примерно 5 % воды, количество которой уменьшается с ростом температуры дегидратации. Если температура не превышает 390 К, выделяется только физически адсорбированная вода, но уже при небольшом нагревании выше этой температуры недиссоциированные молекулы воды взаимодействуют с носителем, образуя гидроксильные группы. После дегидратации при 1070 - 1270 К содержание остаточной воды не превышает нескольких десятых процента. [5]
 |
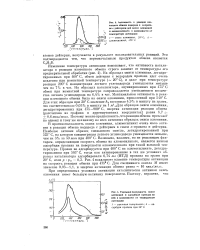
Пики, полученные на колонке с окисью алюминия и сн. ткхаге. [6] |
Для образцов окиси алюминия характерно вымывание на хроматограмме 1-бутена и гракс-2 - бутена в виде одного пика. [7]
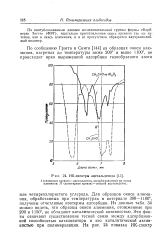 |
ИК-спектры ацетальдегида. [8] |
Для образцов окиси алюминия, обработанных при температурах в интервале 300 - 1100, получены отчетливые изотермы адсорбции. Из данных табл. 34 можно видеть, что образцы окиси алюминия, отожженные при 200 и 1150, не обладают каталитической активностью. Эти факты означают существование тесной связи между адсорбционной способностью катализатора и его каталитической активностью при полимеризации. [9]
На образцах окиси алюминия, дегидратированных при 400 С, обмен дейтерия с водородом пропана идет очень медленно при комнатной температуре ( - 20 С), и даже при температуре реакции 200 С концентрация легкого углеводорода уменьшается меньше чем на 7 % в час. На образцах катализатора, активированных при 475 С обмен при комнатной температуре сопровождается уменьшением количества легкого углеводорода на 6 4 % в час. [11]
При нагревании образца окиси алюминия до 170 в присутствии спирта в спектре появлялись полосы поглощения, которые были отнесены к поверхностным формиат-ионам в случае метанола и поверхностным ацетат-ионам в случае этанола. [12]
Каталитическая активность образцов окиси алюминия, полученных при разных условиях, различна, особенно ниже 400 С. [13]
На практике имеются дегидратированные образцы окиси алюминия с весьма широким диапазоном значений удельной поверхности и среднего размера пор в зависимости от природы исходных веществ, величины их частиц и условий дегидратации; в этом отношении данные де Бура ( см. выше), вероятно, наиболее характерны. [14]
Льюисовские основные центры образцов окиси алюминия также принимают участие в дегидратации первичных и вторичных спиртов путем удаления протона либо от J3 -, либо от у-атома углерода относительно а-углерода, содержащего гидроксильную группу. [15]
Страницы: 1 2 3 4