Образование - диоксан
Cтраница 1
Образование диоксана часто имеет место при катионной полимеризации окиси этилена. [1]
Ацетализация 1 3-диола 55 ацеталем 50 с образованием соответствующего диоксана авторами u использована с целью защиты гидроксильных групп от действия окислителя. [2]
Соответствующие гликоли также дают диоксаны [223], однако образование диоксанов из окиси может происходить непосредственно, минуя гликоль. [3]
Окись этилена подвергается димеризации при нагревании в кислой среде с образованием диоксана ( диэтилен-1 4-диоксид), который представляет собой отличный растворитель для соединения целлюлозы и для смол и жиров. [4]
Одной из важнейших реакций изобутилена является его конденсация с формальдегидом с образованием диоксана и двухатомного спирта, которые при разложении дают изопрен. Реакция конденсации рлефииов с формальдегидом, открытая в 1919 г. Принсом [170], протекает в присутствии минеральных кислот, в частности, в присутствии серной кислоты. [5]
Пентаэритрит может циклизоваться с 1 молем карбонильного соединения в присутствии кислоты с образованием полизамещенного диоксана. Так, из пентаэритрита и ацетона получают 2 2-диметил - 5 5-бш ( оксиметил) - 1 3-диок-сан. [6]
В случае полимеризации окиси этилена одновременно с реакцией роста цепи происходит деполимеризация с образованием диоксана. Сведения об аналогичных процессах при полимеризации замещенных оксиранов и ЭС отсутствуют. Однако мы наблюдали, что в определенных условиях при полимеризации АЭС КТБ не образуется полимер. [7]
Впоследствии Фаворским93 было установлено, что изомеризация окиси этилена под влиянием кислот идет через образование диоксана. [8]
В технической изобутан-изобутиленовой фракции содержатся бутены нормального строения и бутадиен, которые реагируют с формальдегидом с образованием изомер-ных диоксанов. [9]
Сырье для синтеза - изобутиленсодержащая фракция - должна иметь минимальное содержание бутадиена, поскольку он реагирует с формальдегидом с образованием нежелательных изомерных диоксанов. Поэтому из фракции С4 пиролиза первоначально выделяют бутадиен и затем четкой ректификацией основную часть р-бутиленов. [10]
При микроволновом нагреве продолжительность реакции меньше, чем при термическом приблизительно в 2 - 2 5 раза, несмотря на то, что в обоих случаях реакция протекает в открытой системе при одинаковой температуре. Время образования диоксана III составляет 2 5 и 7 ч соответственно для микроволнового и термического нагрева в присутствии серной кислоты. Время его образования с выходом 90 % от теоретического составляет при микроволновом нагреве 45 мин, при термическом - 87 мин. [11]
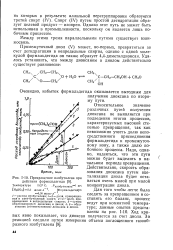 |
Превращение изобутилена при действии формальдегида. [12] |
Действительно, скорость образования диоксана путем аце-тализации диола будет оставаться очень малой при малой концентрации диола. [13]
Известно 48, что при полимеризации окиси этилена в присутствии трехфтористого бора на глубоких стадиях превращения практически единственным продуктом реакции становится диоксан. В присутствии хлорного олова образование диоксана и рост цепи являются параллельными реакциями. В этой же работе 5г приведены данные по образованию ЦТ эпихлор-гидрина и бутиленоксида. [14]
Основные побочные процессы связаны с замещением атома хлора полухлорекса или хлорекса на гидроксид-ион с образованием моновинилового эфира или - хлорэтилового эфира эти-ленгликоля ( ХЭЭ), который претерпевает дегидрохлорирование до моновинилового эфира или быстро вступает в реакцию эфи-рообразования по Вильямсону, поскольку она также ускоряется в условиях МФК. Внутримолекулярная циклизация ХЭЭ приводит к образованию диоксана - основному легкому побочному продукту. При взаимодействии ХЭЭ с молекулой хлорекса происходит димеризация до ди-р ( 5 -дихлорэтилового эфира ди-этиленгликоля ( дихлорекс), последний, в свою очередь, претерпевает дегидрохлорирование до дивинилового эфира диэти-ленгликоля или полудихлорекса. [15]
Страницы: 1 2