Образование - нитрозилсерная кислота
Cтраница 1
Образование нитрозилсерной кислоты сопровождается выделением воды. [1]
Механизм реакции включает образование нитрозилсерной кислоты; последняя гидролизуется с образованием серной кислоты и регенерацией окислов азота. Реакция протекает в камерах или башнях различных типов, в которых предусмотрены устройства для охлаждения и смешения газов, что повышает их производительность. [2]
Указанные выше обратимые реакции приводят к образованию нитрозилсерной кислоты в том случае, если концентрация кислоты достаточно высока, а температура достаточно низка. Лунге, а затем Сорель показали, что такие сернокислые растворы выделяют тем больше нитрозных продуктов, чем менее концентрирована кислота и чем выше температура. [3]
Реакция обнаружения нитритов [124] основана на образовании нитрозилсерной кислоты при взаимодействии нитритов с концентрированной серной кислотой. Нитрозилсерная кислота образует с резорцином резоруфин, ярко флуоресцирующий в щелочном растворе желто-красным светом. [4]
Двуокись азота легко поглощается концентрированной серной кислотой с образованием нитрозилсерной кислоты. При взаимодействии двуокиси азота со щелочами или содой образуются соли азотной или азотистой кислот. [5]
Таким образом, для того чтобы сместить равновесие в сторону образования нитрозилсерной кислоты, нужно вести поглощение окислов азота при более низких температурах, применяя более концентрированную серную кислоту минимальной нитрозности. Для достижения более полного поглощения окислов на орошение пятой башни должна подаваться мало-нитрозная кислота. Что касается концентрации серной кислоты, то при условии, что на орошение пятой башни подается продукционная кислота из первой, башни, не представляется возможным использовать этот фактор для смещения равновесия. В башенной системе циркулирует 75 - 77 % - ная кислота. [6]
Так, в башенном методе получения серной кислоты после поглощения окислов азота гомогенно идет образование нитрозилсерной кислоты. В этом же способе используется и газовая реакция окисления двуокиси серы в трехокись при каталитическом действии газообразных окислов азота. [7]
Смесь равных объемов NO и N02 также растворяется в водных растворах серной кислоты с образованием нитрозилсерной кислоты. [8]
Такое обесцвечивание, сопровождаемое конденсацией кислоты в последней камере, указывает, что либо происходит Образование нитрозилсерной кислоты в результате недостатка воды в первых камерах, либо вследствие избытка последней начинается образование азотной кислоты, сопровождаемое разъедание. [9]
Смесь газов направляют в поглотительные башни, в которых трехокись азота поглощается серной кислотой с образованием нитрозилсерной кислоты. Ее раствор ( нитрозу) снова направляют в продукционную башню на окисление сернистого ангидрида. [10]
На орошение абсорбционных башен подают обычно большее количество серной кислоты, чем это необходимо для связывания окислов азота и образования нитрозилсерной кислоты, вследствие чего последняя растворяется в избытке кислоты и образует нитрозу. [11]
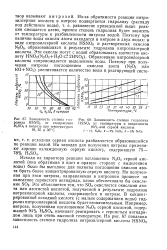 |
Зависимость степени гидролиза HSNO5 от содержания H2SC4 в нитрозе при температурах 19, 35 и 50 С.| Зависимость степени гидролиза HSNOs от температуры и нитрозности. [12] |
Поэтому при наличии воды окислы азота находятся в нитрозе в двух видах: в виде нитрозилсерной кислоты HSNO5 и растворенных окислов N2O3, образовавшихся в результате гидролиза нитрозилсерной кислоты. Образование нитрозилсерной кислоты сопровождается выделением воды. [13]
Окислы азота служат катализатором окисления двуокиси серы в нитрозном способе производства серной кислоты. Механизм реакции включает образование нитрозилсерной кислоты; последняя гидролизуется с образованием серной кислоты и регенерацией окислов азота. Реакция протекает в камерах или башнях различных типов, в которых предусмотрены устройства для охлаждения и смешения газов, что повышает их производительность. [14]
Этот способ основан на образовании нитрозилсерной кислоты H ( NO) SO4, которая окисляет сульфат закисного железа до сульфата окисного железа. Влияние нитрита натрия, если он присутствует в растворе, исключено, так как определение проводят после его удаления в виде этилового эфира азотистой кислоты при кипячении. [15]
Страницы: 1 2