Образование - прочный комплекс
Cтраница 1
Образование прочных комплексов обусловлено в основном силами, связанными с переносом заряда от донора к акцептору. Донорами в органических комплексах с переносом заряда в большинстве случаев являются ароматические углеводороды и некоторые их производные, многоядерные ароматические соединения, полимеры с системой сопряженных связей. Ароматические углеводороды и многие соединения с системой сопряженных связей могут быть не только донорами, но и акцепторами электронов. По отношению к таким веществам донорами электронов являются щелочные металлы [15] и некоторые органические основания. Роль донорно-акцепторного взаимодействия в адгезии полимеров к субстратам различной природы несомненна. [1]
Образование прочных комплексов с различными элементами и избирательность хелатирования, определяемая спецификой донорной способности фосфиновых группировок, обусловливает большую перспективность применения этого типа соединений в аналитической химии, химической технологии, медицине. В процессе выявления конкретных областей применения комплексонов немалую роль играет изучение их маскирующей способности. Важными факторами при маскировании катионов являются рН раствора, концентрации реагентов, кинетика процесса, наличие в реакционной среде других катионов и комплексообразователей, вероятность образования сложных нерастворимых комплексов - полимерных, тройных, биметаллических. [2]
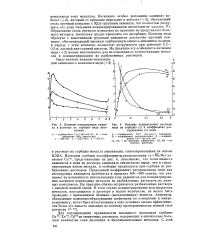 |
Влияние концентрации аммиака в растворе на сорбцию меди анио-нитами.| Влияние концентрации раствора меди на сорбцию ( 1 и коэффициент распределения ( 2 меди. [3] |
Образование столь прочного комплекса на практике не представляет большого интереса, поскольку трудно проводить его десорбцию. [4]
Помимо образования прочных комплексов, по-видимому, могут существовать лабильные комплексы ауксинов с белками. Фрид и другие ( Freed, Reithel, Remmert, 1961) в модельных опытах с кристаллическими ферментами показали, что 2 4 - Д адсорбируется на поверхности молекул ферментов, в результате чего изменялась структура белка, что регистрировалось по характеру флуоресценции. [5]
Возможность образования прочного комплекса 2 2 - ДП с Ре и его активность при окислительно-восстановительных процессах явились предметом исследований со стороны биохимиков и токсикологов. Доза 40 мг / кг является субмаксимальной. Она оказывает переходящее ГД с максимумом через 2 часа. Через 24 часа отмечена фаза незначительной гипогликемии. При подкожном введении крысам 2 2 - ДП ЛД50 равно 131 мг / кг. [6]
На образовании прочных комплексов с ионами тяжелых ме-аллов основано использование и других поли - и гетерофукцио - ( альных тиолов, в частности 2-амино - З - меркапто - З - метилбутано-юй кислоты ( пеницилламин) и 2 3-димеркаптопропансуль - [) оната натрия ( у н и т и о л) в качестве противоядий при отрав - 1ении соединениями тяжелых металлов. [7]
При образовании прочных комплексов условное произведение растворимости сульфида становится столь большим, что образование сульфида металла невозможно. [8]
При образовании очень прочных комплексов с катионами кальция и магния, входящими в состав известкового налета, последний растворяется, и поверхность после смывания продуктов реакции становится совершенно чистой. [9]
При образовании недостаточно прочных комплексов необходимо прибавление значительного избытка реактива, причем последний вводится двумя различными способами. По одному из них реактив прибавляют в некотором кратном отношении к определяемому иону. Этот способ улучшает условия определения, но не обеспечивает его точности. Конечно, всякий избыток реактива уменьшает диссоциацию комплекса, однако при несколько больших разбавлениях прямая пропорциональность между общей концентрацией определяемого иона и оптической плотностью раствора снова заметно нарушается. [10]
При образовании достаточно прочных комплексов п-доноров с о - и - акцепторами наблюдаются, как правило, большие приросты дипольных моментов. Величина перенесенного заряда от донора к акцептору в таких комплексах сравнительно велика и, как показано в гл. I, стабилизацию таких комплексов в основном обусловливают силы переноса заряда. Вклад поляризационного взаимодействия невелик. Для комплексов типа nv и пет наблюдается определенная корреляция между дипольными моментами донорно-акцеп-торных связей и их прочностью. [11]
За счет образования прочных комплексов значительно снижается экстракции скандия в присутствии 0 1 - 0 3 М F -, SQ -, ЭДТА, тартрат-и цитрат-ионов. Как было установлено, присутствие больших количеств аскорбиновой кислоты ( - 1 5 М) не влияет на экстракци-онно-хроматографическое поведение скандия. [12]
РНК недостаточно для образования прочного комплекса, и оно должно быть подкреплено белок-белковым взаимодействием с предварительно связавшимся белком, либо предварительно связавшийся белок наводит ( стабилизирует) локальную конформацию РНК, требуемую для связывания данного белка. [14]
Определение основано на образовании прочного комплекса цинка с ЭДТА. Титрование проводят в слабокислой среде с рН 5 в присутствии индикаторной смеси 1 - ( 2-пиридилазо) - 2-пафтола ( ПАН) и комплексопата меди. При наличии в растворе ионов цинка раствор окрашен в розово-фиолетовый цвет. В конце титрования раствор окрашивается в желтоватый цвет. [15]
Страницы: 1 2 3 4
