Образование - прочный комплекс
Cтраница 2
Определение основано па образовании прочного комплекса цинка с ЭДТА. Титрование проводят в слабокислой среде с рН 5 в присутствии индикаторной смеси 1 - ( 2-пиридилазо) - 2-нафтола ( ПАН) и комплексоната меди. При наличии в растворе ионов цинка раствор окрашен в розово-фиолетовый цвет. В конце титрования раствор окрашивается в желтоватый цвет. [16]
Смешанный механизм, приводящий к образованию прочных комплексов, наблюдается при извлечении металлов кислыми хелатообразующими экстрагентами, напр. [17]
Смешанный механизм, приводящий к образованию прочных комплексов, наблюдается при извлечении из грунта металлических загрязнителей кислыми хелатообразующими экстрагентами или смесями экстрагентов, например кислых и нейтральных. [18]
Смешанный механизм, приводящий к образованию прочных комплексов, наблюдается при извлечении металлов кислыми хелгтообразующими экстратентами, напр. В первом случае образование соли дополняется донорно-акцепторным взаимодействием с участием атома кислорода экстрагента, во втором достигается более полное использование координац. Повышенная прочность комплексов обусловливает увеличение коэф. [19]
Второе обстоятельство, которое способствует образованию прочных комплексов РЗЭ с полидентатными лигандами - это их высокий заряд. [20]
Растворители апротонные, не способные к образованию прочных комплексов в растворе, неполярные или малополярные и с малой диэлектрической проницаемостью. [21]
Гистерезис, возможно, связан с образованием прочных комплексов дэпитов с молекулами метанола. [23]
Это может иметь место только в случае образования прочных комплексов. Кроме того, связывание определяемого иона в прочный комплекс не требует большого избытка реактива. Преимущество прочных комплексов также в том, что они сохраняют постоянный состав в больших интервалах концентраций реактива и других компонентов. [24]
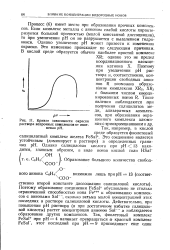 |
Кривая зависимости окраски раствора непрочных комплексов от изменения рН. [25] |
Процесс ( б) имеет место при образовании прочных комплексов. Если комплекс металла с анионом слабой кислоты характеризуется большой прочностью ( малой константой диссоциации), то при увеличении рН он не разрушается с выделением гидроокиси. Однако увеличение рН может привести к изменению окраски. Это изменение происходит по следующим причинам. [26]
В отдельных случаях гидратация ионов может приводить к образованию довольно прочных комплексов. [27]
 |
Кривая насыщения для случая образования прочного комплекса. [28] |
Метод молярных отношений [1 ] является наиболее общим приемом исследования образования прочных комплексов. Суть метода заключается в измерении величины D ( или AD) для растворов с различным отношением СА / СМ при постоянной концентрации См и наоборот. [29]
Выяснено, что пассивирующее влияние электроотрицательных групп реагентов определяется образованием прочных комплексов с катализатором. Найдены пути преодоления этого влияния. [30]
Страницы: 1 2 3 4
