Образование - сольватный комплекс
Cтраница 1
Образование сольватных комплексов осуществляется посредством водородной связи. При этом в роли акцептора протона выступает кислород. [1]
Образование сольватных комплексов сопровождается появлением новых скелетных колебаний. Присоединение молекулы растворителя к молекуле растворенного соединения приводит к изменению ( в общем случае уменьшению) симметрии обоих реагентов. Это изменяет ( обычно увеличивает) число активных в ИК-спектре колебаний. Известно, что активными в ИК-спектре являются только такие колебания, которые связаны с изменениями дипольных моментов молекул. Понятно, что уменьшение симметрии молекул приводит к увеличению числа таких колебаний. [2]
Образование сольватных комплексов происходит за счет делокализа-ции электронов донорных орбиталей электроотрицательных атомов молекул растворителя на акцепторные орбитали катионов. Для анионов сольватация та же, но донором электронов выступает анион, а акцептором - протон молекулы растворителя. Связь между анионом и молекулой растворителя реализуется по типу водородной. Энергетическая равноценность связей в сольватных комплексах предполагает гибридизацию орбиталей катионов и анионов, тип которой в свою очередь определяет геометрическую структуру комплексов и координационные числа ионов. Таким образом, исходя из квантовомеханической теории ствие ионов с молекулами воды, спиртов, аммиака, карбоновых кислот частично ковалентное, а не кулоновское и ион-дипольное. Вклад ковалентных взаимодействий значителен в случае ионов малого размера, а также ионов незаполненными электронными оболочками. Единый механизм сольватации одних и тех же ионов в растворителях подтверждается постоянством энергии Так, например, для раствора NaCl в воде и метаноле получено ние порядка 731 5 кДж / моль; для KI в тех же растворителях получается 610 и 593 кДж / моль соответственно. [3]
Как уже отмечалось, образование сольватных комплексов между растворителем и молекулами реагента, с которым взаимодействует свободный радикал, также приводит к снижению наблюдаемой константы скорости реакции. Аналогичные эффекты имеют место и при наличии в системе автоассоциатов реагирующих молекул, образующихся обычно за счет водородной связи. В частности, показано [59], что в реакции метильных радикалов со спиртами, протекающей путем отрыва атома водорода от гидроксильной группы, реакционноспособными оказываются только мономерные молекулы спирта. Автоассоциация в инертной среде, зависящая от концентрации спирта в системе, замедляет скорость замещения. [4]
Экспериментальные данные показывают, что при сильном энергетическом взаимодействии между молекулами растворителя и полимера с образованием сольватных комплексов процесс растворения не всегда проходит до конца, останавливаясь на стадии ограниченного набухания. При сильном взаимодействии молекулы растворителя могут располагаться в строго упорядоченном состоянии по местам активных атомов или групп полимерных цепей, с которыми молекулы растворителя образуют сольватные комплексы. Следовательно, число микросостояний молекул растворителя резко снижается по сравнению с числом микросостояний их в самом растворителе. [5]
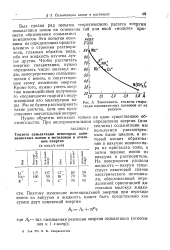 |
Зависимость теплоты гидратации одновалентных катионов от их. [6] |
Был сделан ряд попыток теоретического расчета энергии сольватации ионов на основании той или иной модели процесса образования сольватных комплексов. Эти попытки основаны на определенных представлениях о строении растворителя, главным образом воды, ибо эта жидкость изучена лучше других. Чтобы рассчитать энергию сольватации, нужно определить число молекул воды, непосредственно связывающихся с ионом, и сопутствующее этому изменение энергии. [7]
 |
Теплота гидратации ионов по данным К. П. Мищенко. [8] |
Был сделан ряд попыток теоретического расчета энергии сольватации ионов на основании той или иной модели процесса образования сольватных комплексов. [9]
При растворении акцепторного соединения АХД, например SbClu, в донорном растворителе D по схеме [1] происходит образование сольватного комплекса. Сольватный комплекс может затем реагировать с конкурирующим лигандом L. Реакции замещения такого типа могут осуществляться а) при добавлении более сильного, чем растворитель, донора или б) благодаря смещению равновесия вследствие различий в летучести, растворимости или при добавлении большого избытка замещающего донора. Образование аммиакатов некоторых переходных металлов в водном растворе осуществляется в соответствии с пунктом а) и обусловлено более сильными донорными свойствами аммиака по сравнению с водой, хотя вода благодаря ее меньшей летучести по сравнению с аммиаком может быть в избытке. [10]
Глюкауф и Мак-Кей [110] первыми предположили, что хорошая экстракция уранил-иона и его аналогов связана с использованием при образовании сольватного комплекса 5f - op - бит, однако Кацин [170] отметил, что основные органические растворители могут сольватировать ряд неорганических нитратов, так что нитрат уранила никоим образом нельзя считать уникальным. Качественно это, несомненно, правильно, но различия представляются довольно большими. Конник и Югус [43] предположили, что вследствие особой структуры уранил-иона атом урана несет, по существу, заряд 4 и что этот высокий заряд может быть ответственным за сильное взаимодействие с основными растворителями. [11]
Часто на основании лишь экспериментальных данных о различных проявлениях сольватации ионов нельзя однозначно определить тип сольватации и рассчитать энергетику образования сольватных комплексов. [12]
Такая зависимость наблюдается экспериментально часто ( так называемое асимметричное уширение) и может служить указанием на то, что в таких случаях действительно вероятно образование сольватных комплексов - микрокристаллов вокруг парамагнитной частицы. Однако это условие вовсе не обязательно и не всегда выполняется. [13]
Ими выведено уравнение, позволяющее определить величину коэффициента распределения урана ( Л) во всей области кислотности при экст ракции Д2ЭШК, и отрицается образование чисто сольватного комплекса, ввиду слабых электронодонорных свойств фосфоридьного кислорода. [14]
При данной константе образования анионного комплекса К3 в растворителе с сильными до норными свойствами значения sbcif будут невелики, так как при этом константа образования сольватного комплекса К будет иметь высокие значения. [15]
Страницы: 1 2