Образование - малорастворимые осадки
Cтраница 1
Образование малорастворимых осадков при взаимодействии растворов исследуемых композиций с пластовыми водами оказывает дополнительное положительное влияние на увеличение фильтрационного сопротивления водонасыщенных зон пласта. [1]
Метод меркурометрии основан на образовании малорастворимых осадков солей закиси ртути. Комплексный катион Hga по современным представлениям имеет строение [ Hg2 ( Hg) ] 2, таким образом, этот катион содержит в своем составе ион двухвалентной ртути и атом металлической ртути и получается при поляризационном взаимодействии этих двух частиц. Полученный раствор нитрата закиси ртути хранится в склянках из темного стекла. По сравнению с раствором AgNO3 растворы Hg2 ( NO3) 2 имеют некоторые преимущества. При хранении в течение года концентрация растворов Hg2 ( NO3) 2 практически не изменяется. [2]
Амперометрическое титрование сульфат-иона основано на образовании малорастворимых осадков и главным образом на образовании сульфата свинца. [3]
Осадочная хроматография - разделение веществ вследствие образования малорастворимых осадков в определенном порядке, который обусловливается их растворимостью. [4]
Физико-химическая кольматация истинными растворами основана на образовании малорастворимых осадков, являющихся продуктами химического взаимодействия химических реагентов друг с другом, солями пластовых вод или с породой пласта. Электролит выпадает в осадок при соотношении, когда произведение растворимости продукта меньше произведения концентраций ионов с учетом влияния пластовых условий. Например, температура на растворимость солей влияет различно, что объясняется тепловым эффектом растворения. Одни соли при растворении поглощают тепло, другие - выделяют. [5]
Написать в ионно-молекулярной форме уравнения реакций, приводящих к образованию малорастворимых осадков или газов: a) Pb ( NO3) 2 KI; б) NiCl2 H2S; в) КаСОз НС. [6]
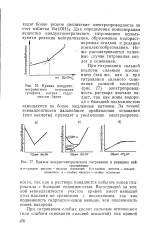 |
Кривая кондукто-метрического титрования сульфата натрия гидроокисью бария.| Кривые кондуктометрического титрования в реакциях нейтрализации. [7] |
Для определения концентрации вещества кондуктометрическим титрованием используются реакции нейтрализации, образования малорастворимых осадков и реакции комплексообразования. Ниже рассматриваются типичные случаи титрования кислот и оснований. [8]
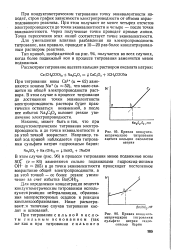 |
Кривая кондукто.| Кривая кондукто-метрического титрования сульфата натрия гидроокисью бария. [9] |
Для определения концентрации веществ кондуктометрическим титрованием используются реакции нейтрализации, образования малорастворимых осадков и реакции комплексообразования. Ниже расматри-вают: я типичные случаи титрования кислот и оснований. [10]
 |
Индикаторы для титрования сульфатов раствором соли бария. [11] |
Титрование растворами солей свинца - плюмбомет-рия - протекает обычно с образованием малорастворимых осадков. Индикация окончания реакции может происходить по двум механизмам. [12]
На нефтяных и газовых месторождениях одним из распространенных видов агрессии, сопровождающихся образованием малорастворимых осадков, является сероводородная. [13]
 |
Устойчивость сернистого ангидрида к. [14] |
Сероводород и меркаптаны, которые могут присутствовать в газах, также поглощаются этим раствором с образованием малорастворимых осадков. Эти осадки легко so мкз / мл могут быть отделены от раствора декантацией или фильтрованием. [15]
Страницы: 1 2