Образование - полугидрат
Cтраница 2
Размеры выделяющихся кристаллов сульфата кальция при различных условиях изучены в большей мере при образовании гипса и в меньшей - при образовании полугидрата и ангидрита. Установлено [57 ], что с повышением температуры от 30 до 80 при выделении гипса из фосфорнокислых растворов увеличивается длина кристаллов в 10 - 15 раз, а ширина их в 3 - 5 раз. С изменением концентрации кислоты от 25 до 34 % Р205 продольные и поперечные размеры кристаллов значительно уменьшаются. [16]
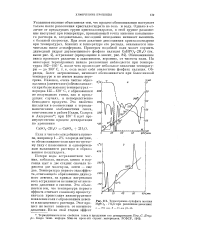 |
Тормограмма сульфата магния MgS04 ТНоОпри различном давлении. [17] |
Если к чистой соли добавить примеси, например 1 - 2 % хлорида натрия, то обезвоживание соли идет по третьему типу с плавлением и одновременным выкипанием раствора и образованием полугидрата. [18]
Получают в виде р-формы. Способна гидратиро-ваться с образованием полугидрата ( и дигидрата) при темп. [19]
В присутствии небольших количеств воды температура плавления кислоты понижается, и кристаллизация ее замедляется. Она ускоряется при образовании полугидрата Н3РО4 - 0 5Н2О, плавящегося при 29 32 С. [20]
В производственных условиях в котлах наблюдается кипение. Первое кипение порошка происходит при температуре 120 - 150 и характеризуется в основном образованием полугидрата. Во время второго кипения, наблюдаемого при 170 - 190, образуется обезвоженный полугидрат. Выделяющийся пар обволакивает отдельные зерна материала и вызывает заметное увеличение подвижности массы. При совмещенном помоле и обжиге гипса применяются высокие температуры печного пространства, так как продолжительность пребывания частиц в зоне температурного воздействия незначительна. [21]
При варке из материала выделяются пары воды, причем подвижность порошка подобна подвижности жидкости. Первое кипение гипсового порошка происходит при температуре 140 - 150 С и характеризуется в основном образованием полугидрата, второе - при 170 - 190 С и сопровождается полным обезвоживанием полугидрата. Вторая осадка менее интенсивна. [22]
Эта схема объясняет получение 7 рег-бутиладищшовой кислоты через стадию образования 2-нитро - 4-трет-бутилциклогексаиона, при нит-розировании которого и образуется карбоксинитроловая кислота. Основная причина уменьшения селективности реакции окисления 4 - ТБЦГола, как и в случае циклогексанола, состоит в том, что наряду с нитросоединениями образуются изомерные им эфиры азотистой кислоты, которые через стадию образования полугидрата трет-бутилцикло-гександиона превращаются в низшие гомологи дикарбоновых кислот, монокарбоновые кислоты и углекислый газ. [23]
На заводах температура обжига строительного гипса в варочных котлах обычно составляет 413 - 463 К. В производственных условиях из-за быстрого выделения паров воды в котлах наблюдается кипение порошка. Первое кипение порошка происходит при температуре 413 - 423 К и характеризуется в основном образованием полугидрата. Во время второго кипения, наблюдаемого при температуре 443 - 463 К, образуется обезвоженный полугидрат. Выделяющийся пар обволакивает отдельные зерна материала и вызывает резкое увеличение их подвижности. [24]
При использовании отвального фосфогипса с влажностью 30 - 40 % необходима его сушка. Снижение влажности фосфогипса чаще всего достигается путем прямого испарения, на что расходуется в 1 5 - 2 0 раза больше топлива, чем на получение гипсового вяжущего из природного сырья. При этом себестоимость товарного фосфогипса в 2 5 - 3 5 раза превышает себестоимость добычи и переработки природного гипсового камня. Сушка в низкотемпературном режиме применяется в связи с влиянием кислых примесей фосфогипса на температуру дегидратации. Исследования дегидратации непромытого фосфогипса, проведенные в широком интервале кислотности, показали, что под влиянием кислых фосфатных и фтористых соединений температура образования полугидрата, растворимого и нерастворимого ангидрита снижается. Причем подавляющая доля нерастворимого ангидрита образуется преимущественно при низких температурах. [25]
 |
Термограмма пентагидрата меди. [26] |
Дюваля [124] изложены результаты обширных исследований пиролитического разложения неорганических и ме-таллоорганических соединений. Установлены состав и термическая стабильность многих веществ, образующихся в виде осадков при гравиметрическом анализе неорганических материалов. Описаны подробные исследования термического распада пентагидрата сульфата меди. При нагревании примерно до 40 С, по-видимому, происходит потеря двух молей воды. Дальнейшее нагревание до 70 С приводит к потере еще двух молей воды. Образующийся при этом моногидрат стабилен до температуры 250 С. В интервале 250 - 300 С соль становится безводной. Какие-либо свидетельства в пользу образования полугидрата отсутствуют. [27]
Страницы: 1 2