Образование - координационная связь
Cтраница 2
При образовании координационных связей между ионом металла и лигандом свойства того и другого могут изменяться в различных случаях по-разному. Часто органический лиганд приобретает устойчивость по отношению к гидролизу, воздействию химических реагентов и нагреванию. [16]
При образовании координационной связи электронодонорный атом уже не владеет полностью отданной парой электронов и приобретает, таким образом, положительный заряд; аналогично электроноакцептор-ный атом обладает теперь некоторым избытком электронов относительно его ядерного заряда, так что он приобретает ( формальный) отрицательный заряд. [17]
При образовании координационных связей атомами кислорода или азота значения частот v ( СН) закономерно возрастают с ростом прочности ( степени ковалентности) этих связей. На ряде примеров показано, что частоты v ( CH) могут быть использованы в качестве критерия образования и прочности координационных связей для решения задач структурной химии. [18]
При образовании координационной связи электронодонорный атом уже не владеет полностью отданной парой электронов и приобретает, таким образом, положительный заряд; аналогично электроноакцептор-ный атом обладает теперь некоторым избытком электронов относительно его ядерного заряда, так что он приобретает ( формальный) отрицательный заряд. [19]
В образовании координационной связи могут участвовать не только атомы, но и ионы. [20]
При образовании координационной связи ( по схемам I и II) вода остается еще в виде молекулы, хотя затягивание ее пары электронов на d - op - биту атома кремния приводит, по-видимому, к значительной протониза-ции атомов водорода молекулы воды, в результате чего она обладает измененными, более кислыми свойствами. [21]
В пользу образования координационной связи за счет фосфо-рильного кислорода говорит исчезновение в ИК-спектре продукта I полосы 1280 см 1, отвечающей колебаниям Р - О-группы в МСФ [6], и появление полосы в области 1210 - 1220 см 1, характерной для координированной Р - О-группы. [22]
Если при образовании координационных связей между ионами металла и водой выделяется энергия, то это может сместить равновесие в сторону процесса растворения. [23]
Поскольку в образовании координационной связи участвуют электроны лигандов, постольку очень существенна электроотрицательность поел ед них, от. Насколько менее электроотрицателен лиганд, настолько легче возникает ковалентная связь и настолько устойчивее обрадованный комплекс. [24]
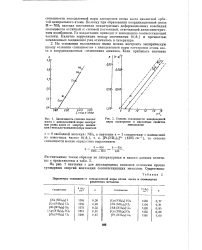 |
Зависимость степени связанности s неподеленной пары электронов атома азота от энергии ионизации / мета лла-комплексообра зователя.| Степень связанности неподеленной. [25] |
Поэтому при образовании координационной связи M - f - NH3 силовая постоянная симметричных деформационных колебаний оказывается отличной от силовой постоянной, отвечающей антисимметричным колебаниям. Ее воз растание приводит к повышению соответствующей частоты. [26]
Во многих случаях образование координационной связи, которая по теории Льюиса возникает в результате реакции нейтрализации, с точки зрения классических теорий относится к окислительно-восстановительным реакциям. [27]
Некоторые другие примеры образования координационных связей, а также некоторые другие типы связей ( как водородная связь) будут рассмотрены в дальнейшем. [28]
Основным фактором, обусловливающим образование координационной связи в фазе комплекситов, является наличие свободных или одноэлектронных орбиталей у ионов металла и его стремление покрыть свой электронный дефицит за счет электронных пар донора, входящего в состав функциональных групп полимера. [29]
Одной о-оксигруппы недостаточно для образования прочной координационной связи хрома с атомом азота в азогруппе; это также относится к железу, марганцу и цинку в отличие от меди, никеля и кобальта, которые образуют координационные комплексы с о-оксиазосоединениями. Хромовые комплексы о о - диоксиазокрасителей обладают значительно большей прочностью к действию минеральных кислот и щелочей, чем соответствующие производные меди. Особые свойства хромовых комплексов о о - ди-оксиазокрасителей объясняют причины преимущественного использования хрома для кислотных протравных азокрасителей для шерсти и тот факт, что красители, приобретающие после хромирования наибольшую прочность, содержат две оксигруппы, обязательно в о-положениях к азогруппе. [30]
Страницы: 1 2 3 4