Образование - тройная связь
Cтраница 1
Образование тройной связи невозможно, так как один атом хлора связан с третичным атомом углерода. [1]
Образование тройной связи протекает по аналогичным правилам. Так, дегидрогалоидирование непредельных галоидопроизвод-ных под действием щелочных агентов протекает наиболее легко для соединений V или VI, у которых атомы хлора и водорода находятся в транс-положении. [2]
 |
Молекула этилена.| Схема образования я-связи. [3] |
Образование тройной связи связано с sp - гибридизацией. В этом случае смешиваются друг с другом одна s - орбиталь и одна р-орбиталь, образуя две гибридные орбитали. [4]
Образование тройной связи происходит со значительно большей скоростью в том случае, когда отщепляющиеся атомы занимают транс -, а не zfMC - положение. Так, хлор-фумаровая кислота превращается в присутствии щелочей в ацетиленди-карбоновую кислоту примерно в 50 раз быстрее, чем хлормалеиновая кислота ( А. [5]
В образовании тройной связи принимают участие три пары валентных электронов, причем эти три пары электронов неравноценны. Одна из них того же типа, что и в обычной, ординарной ст-связи С - С, остальные две принадлежат к другому типу, так же как и вторая электронная пара в двойной связи, - это электроны я-связн ( см. стр. [6]
В образовании тройной связи принимают участие три пары валентных электронов, причем эти три пары электронов неравноценны. Одна из них того же типа, что и в обычной, ординарной о-связи С - С, остальные две принадлежат к другому типу, так же как и вторая электронная пара в двойной связи, - это электроны я-связи ( см. стр. [7]
 |
Схема 92Р2 - гибридизации [ IMAGE ] Схема строения нитевид-атома углерода ных кристаллов карбина. [8] |
При образовании тройной связи между углеродными атомами - ( а 2л) - связи - в гомологическом ряду непредельных углеводородов типа ацетилена увеличивается энергия связи и уменьшается расстояние между атомами С. [9]
Элиминирование происходит также с образованием тройных связей, это показано на примере реакций цис - и транс - НООС-СН СС1 - СООН. [10]
Простой и широко используемый метод образования тройной связи углерод-азот состоит в отщеплении воды от первичных карбоксамидов. [11]
Это упрочнение идет за счет образования тройной связи, что невозможно в случае молекулы О2, и так уже перегруженной антисвязевыми электронами. [12]
Структура кетоксимов обычно не позволяет осуществить образование тройной связи углерод-азот за счет реакции отщепления. Однако наличие а-заместителей, таких, как карбонильная, амино -, гидрокси - или алкоксигруппа, так называемые электроно-донорные группы [499], способствует их распаду по Бекману [74, 309, 454, 499] с образованием нитрилов при нагревании или в присутствии таких агентов, как пентахлорид фосфора, тионилхло-рид, полифосфорная кислота. [13]
В результате между атомами галогенов возможно образование тройной связи: одной ах и двух л во взаимно перпендикулярных плоскостях - XY и XZ. Этой возможности лишены атомы фтора, не имеющие вакантных d - орбиталей. [14]
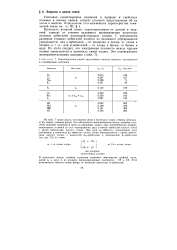 |
Характеристики связей двухатомных молекул веществ, находящихся в газообразном состоянии. [15] |
Страницы: 1 2 3 4