Образование - смешанная соль
Cтраница 1
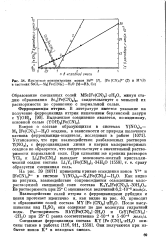 |
Изменение концентрации ионов Sc3 ( 1, [ Fe ( CN6 ] 4 - ( 2 и М ( 3 в системах ScCl3 - M4 [ Fe ( CN e ] - № 0 ( MRb, Cs. [1] |
Образование смешанных солей MSc [ Fe ( CN) 6 ] - a: H20, минуя стадию образования Sc4 [ Fe ( CN) e ] 3, свидетельствует о меньшей их растворимости до сравнению с нормальной солью. [2]
Приведенные кривые свидетельствуют о том, что для Zr образование смешанных солей с тяжелыми щелочными металлами нехарактерно. [3]
 |
Смешанные ферроцианиды кобальта. [4] |
Это выражается в заметном отклонении линии осаждения в сторону образования смешанных солей. При значительном избытке Nia ( n 0 15) осаждается Ni [ Fe ( CN) e ], который в интервале 0 15 [ п ] 0 7 поглощает избыточные количества Na4 [ Fe ( CN) 6 ] с образованием твердого раствора. [5]
Частичная нейтрализация кислоты одним ос-нованлем с последующей ее нейтрализацией другим основанием приводит к образованию смешанных солей. [6]
 |
Участок струк - г. [7] |
При наличии в растворе одновременно двух малодиссоциированных галидов ртути между ними происходит частичное обменное взаимодействие с образованием смешанных солей. Так, с помощью ультрафиолетовой спектроскопии было показано, что в 0 001 М растворе HCIO4 константы равновесия реакций по схеме Hgr2 Hgr 2HgIT равны 14 ( С. [8]
 |
Изменение состава осадка в системе NIS04 - Li4 [ Fe ( CN6 ] - Н20.| Смешанные ферроцианиды никеля. [9] |
Из изложенного выше следует, что нормальный ферроцианид никеля весьма склонен к реакции присоединения ферроцианидов щелочных металлов с образованием смешанных солей. [10]
Напротив, в присутствии калиевых солей растворимость ферроцианида натрия заметно увеличивается [413], что связано, по-видимому, с образованием смешанных солей. В абсолютном спирте Железистосинеродистый натрий практически нерастворим. [11]
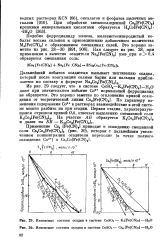 |
Изменение состава осадка в системе CoS04 - Ki [ Fe ( CN e ] - [ IMAGE ] Изменение состава осадка в системе CoSOi - Cs4 [ Fe ( CN e ] - Н2О. [12] |
Подобно ферроцианиду железа, железистосинеродистый кобальт весьма склонен к присоединению добавочного количества M4 [ Fe ( CN) e ] с образованием смешанных солей. [13]
В интервале молярных отношений M4 [ Fe ( CN) e ]: AgN03 0 25 - 0 50 наблюдается последовательное внедрение в осадок ионов тяжелого щелочного металла с образованием смешанных солей MAg3 [ Fe ( CN) e ] и M2Ag2 [ Fe ( CN) 6 ], где М - рубидий или цезий. [14]
Работы по изучению комплексных оксалатов четырехвалентного урана и тория, проводившиеся под руководством А. А. Гринберга, представляют интерес прежде всего с точки зрения общих вопросов химии комплексных соединений, ибо U ( IV) и Th являются представителями немногочисленной группы металлов, характеризующихся высокими координационными числами ( больше 6); они способны давать высокозаряженные анионы и склонны к образованию смешанных солей. Сравнительное изучение производных урана и тория важно с точки зрения дальнейшего развития химии актинидов. [15]
Страницы: 1 2