Образование - хлорид - железо
Cтраница 1
Образование хлоридов железа и их растворение в хлорной воде являются основными причинами усиленной коррозии металлов в среде влажного хлора, в частности коррозии углеродистых сталей. [1]
При хлорировании ферросилиция и феррованадия изменения изобарных потенциалов реакций образования хлоридов железа, кремния и ванадия ( на 1 г / атом хлора) примерно одинаковы. Соответственно в равной степени хлорируются отдельные компоненты этих сплавов. [2]
 |
Схема производства безводного хлорида железа ( III. [3] |
При нагревании в вакууме выше 500 С хлорид железа ( III) частично разлагается с образованием хлорида железа ( II) и элементарного хлора. [4]
Установлено [6], что активная сера в присадке, сочетающей соединения серы и хлора, ускоряет образование хлоридов железа; наоборот, образование сульфидов железа в присутствии хлорных компонентов уменьшается. [5]
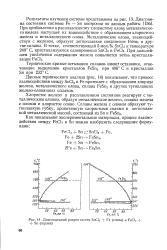 |
Диагональный разрез систем SnCb - f Fe ( слева и Fed. - j - Sn ( справа. [6] |
Данные термического анализа ( рис. 14) показывают, что процесс взаимодействия между SnCl2 и Fe протекает с образованием хлорида железа, металлического олова, сплава FeSn2 и других тугоплавких железо-оловянных сплавов. [7]
При действии сероводорода на железо образуется пленка сернистого железа, которая защищает металл от дальнейшего растворения, однако легко разрушается под воздействием хлористого водорода с образованием хлорида железа, растворимого в воде. Выделяющий при этом сероводород вновь вступает в реакцию с железом, разрушая его, т.е. служит как бы катализатором его растворения. Поэтому из данной реакции необходимо вывести один из коррозионно-агрессивных компонентов. Наиболее легко осуществить перевод хлор-ионов в негидролизу-емый хлорид натрия путем защелачивания нефти. [8]
Образующаяся в процессе гидролиза хлора соляная кислота легко вступает во взаимодействие с железом, сопровождающееся образованием трихлорида железа РеС13 и дихлорида железа FeClz, которые хорошо растворимы в хлорной воде. Образование хлоридов железа протекает со значительной скоростью даже при температурах, заметно превышающих точку росы, поскольку хлориды железа являются гигроскопичными продуктами и конденсация влаги из газа идет и при этих температурах. [9]
Следует обратить внимание на то, что сколько бы ни прибавлять хлорида калия, полностью обесцветить раствор роданида железа не удастся; это значит, что все же в растворе будет находиться некоторое его количество, так как оно образуется за счет прямой реакции. Как только пойдет образование хлорида железа и роданида калия, они тотчас же вступят друг с другом в реакцию и вновь дадут некоторое количество роданида железа. [10]
Высокое содержание железа затрудняет получение хлорида титана из ильменита. При прямом хлорировании концентрата на образование хлорида железа затрачивается миого хлора. Кроме того, большие количества образующегося хлорного железа трудно утилизировать. [11]
При концентрации хлоридов более 300 мг л - 1 вода приобретает солоноватый привкус. Кроме того, хлориды усиливают коррозию железа в воде вследствие образования хорошо растворимого хлорида железа. [12]
 |
Ротор хлорного турбокомпрессора через 20 - 30 минут после попадания в газовый тракт воды ( рабочие колеса первой ступени полностью разрушены. [13] |
При растворении хлора в воде образуется хлорная вода ( см. стр. Под действием последних железо и его сплавы сильно корродируют с образованием хлоридов железа, забивающих протоки и коммуникации хлорных компрессоров. [14]
Хлорид железа при введении в окисляемое сырье практически нацедо разлагается уже в первую минуту окисления. Железо из трехвалентного переходит в двухвалентное состояние, возможно, в результате взаимодействия его и углеводорода с образованием хлорида железа, хлорида водорода и углеводородного радикала. Это создает самостоятельную цепь образования продуктов окисления и уплотнения. [15]
Страницы: 1 2