Образование - начальный активный центр
Cтраница 2
Индивидуальные особенности каждой конкретной полимери-зующейся системы определяются прежде всего природой агента, вызывающего образование начальных активных центров. Эти центры могут быть либо свободными радикалами, либо ионами. Поэтому различают процессы радикальной, катионной и анионной полимеризации, в которых растущие цепи представляют собой макрорадикалы, макрокатионы или макроанионы. При ионной полимеризации растущие цепи далеко не всегда могут рассматриваться как свободные ионы. [16]
Приведенные данные показывают, что при инициировании цепных реакций ионизирующей радиацией происходит не только образование начальных активных центров, но может изменяться и механизм развития реакционной цепи. [17]
Это усугубляется дополнительными факторами, в частности различиями-иногда весьма существенными - между инициатором как источником образования начальных активных центров и растущими цепями, а также способностью многих частиц ионной природы к комплексо-образованию. Параллельное существование и взаимные переходы различных активных центров приводят уже при исследовании простейших ионных систем к необходимости выбора между возможными типами центров инициирования и роста или оценки их относительной активности. Для систем, содержащих переходные металлы, альтернативным может оказаться даже отнесение активных центров к ионному или радикальному типу. [18]
Рассмотренные данные дают основание для вывода, что при возбуждении цепных реакций ионизирующей радиацией происходит не только образование начальных активных центров, но может изменяться самый механизм развития реакционной цепи. [19]
Рассмотренные данные дают основание для вывода, что при возбуждении цепных реакций ионизирующей радиацией происходит не только образование начальных активных центров, но может изменяться самый механизм развития реакционной цепи. [20]
При синтезе макромолекул с высоким молекулярным весом расход мономеров на реакцию роста значительно превосходит расход на реакции образования начального активного центра, обрыва и передачи цепи. [21]
Высказано предположение, что наличие индукционного периода процессов образования кислот, эфиров и карбонильных соединений при поглощении небольших количеств кислорода означает образование начальных активных центров в первой стадии окисления. [22]
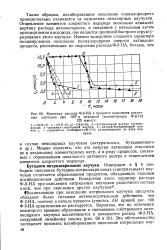 |
Кинетика расхода Ф - - НА в процессе окисления различных каучуков при 120 и исходной [ концентрации Ф - - НА. [23] |
Можно полагать, что эта энергия активации относится не к начальному элементарному акту, а к ряду процессов, связанных с образованием начального активного центра и отщеплением элементов хлористого водорода. [24]
Кинетические исследования обычно проводят при низкой конверсии мономеров, чтобы избежать необходимости учета реакций разветвления полимеров. Принимается принцип квазистационарного состояния, при котором скорость образования начальных активных центров полимеризации равна скорости обрыва цепи путем рекомбинации. [25]
Существуют различные способы классификации полимеризационных процессов. Так, в зависимости от природы агента, вызывающего образование начального активного центра, различают [11] процессы радикальной полимеризации и ионной, которая, в свою очередь, делится на катионную и анионную. [26]
Необходимо указать, что способность к полимеризации аллиловых эфиров кислот фосфора иногда ведет к авариям во время их перегонки, особенно если вещество предварительно недостаточно хорошо промыто и высушено. Длительное нагревание, даже в присутствии ингибиторов, сопровождается частичным разложением вещества и образованием начальных активных центров полимеризации, число которых постепенно увеличивается. [27]
Обычно принимается, что влияние солей металлов переменной валентности на процесс окисления углеводородов обусловлено только генерированием начальных активных центров за счет ускорения распада гидроперекиси. Выше уже было отмечено, что реакция восстановления солей железа и хрома углеводородами приводит к инициированию радикальных процессов. Выше 100 весьма существенная роль в образовании начальных активных центров может принадлежать не только реакциям распада гидроперекиси, а реакциям, в которых углеводород является восстановителем, а окисные соли металлов - окислителями. [28]
Осуществляется в газообразной, жидкой или твердой фазе. В первом случае свет служит только для инициирования р-ции ( образования начальных активных центров в результате перевода молекул мономера или инициатора в возбужд. В пром-сти используется гл. [29]
Осуществляется в гззос5 азной, жидкой или твердой фазе. В первом случае свет служит только для инициирования р-ции ( образования начальных активных центров в результате перевода молекул мономера или инициатора в возбужд. В пром-сти используется гл. [30]
Страницы: 1 2 3