Образование - цианамид - кальций
Cтраница 1
Образование цианамида кальция требует большого расхода теплоты, выход продукта невелик, и роль этого метода в промышленности связанного азота незначительная. [1]
Исследование кинетических закономерностей процесса образования цианамида кальция из цианистого водорода и оксида к а л ь ц и я проводилось в дифференциальном реакторе с малыми навесками и тонким слоем твердого вещества, вдоль высоты которого концентрация газообразного реагента изменялась незначительно. Для наблюдения за кинетикой процесса был выбран гравиметрический метод, обеспечивающий безинерционность измерения и позволяющий быстро, а также удобно фиксировать глубину протекания реакции в твердом образце в любой момент времени. [2]
 |
Давление азота в системе CaCN2 - N2 в зависимости от степени азотирования карбида кальция. [3] |
На рис. 453 представлена изобара реакции образования цианамида кальция при атмосферном давлении. [4]
 |
Давление азота в системе CaCN2 - N2 в зависимости от степени азотирования карбида кальция. [5] |
На рис. 403 представлена изобара реакции образования цианамида кальция при атмосферном давлении. [6]
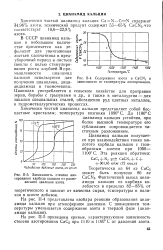 |
Содержание азота в CaCN2 в зависимости от температуры азотирования. [7] |
На рис. П-4 представлена изобара реакции образования цианамида кальция при атмосферном давлении. [8]
При высокой температуре карбид кальция реагирует с азотом с образованием цианамида кальция CaCN2 и выделением углерода в свободном состоянии. [9]
Хотя исторически метод фиксации атмосферного азота путем присоединения его к карбиду кальция с образованием цианамида кальция предшествовал синтезу А. Перспективы дальнейшего развития циан-амидного метода ныне не обещают каких-либо значительных сокращений стоимости производства, к-рые могли бы вернуть ему преимущественную роль. Цнанамидный способ фиксации азота ( по идее Франка и Каро) основан на способности нарбида кальция при t ок. Достаточно нагреть перемолотый в порошок карбид лишь для начала реакции до 1 000, н дальнейший процесс присоединения N2 идет самостоятельно не только без затраты тепла, но даже с его выделением. [10]
Нагревание соединений кальция с углеродом и связанным азотом выше 500 С обычно приводит к образованию цианамида кальция; его получали из окиси кальция и мочевины, гуанидина, дициандиамида или мелама и из нитрида кальция и углерода. Три лабораторных способа приготовления чистого цианамида кальция описаны на стр. [11]
Скорость обратной реакции очень быстро возрастает с повышением температуры, а скорость прямой реакции снижается: при 1400 образование цианамида кальция практически прекращается. [12]
Сущность цианамидного метода заключается в том, что тонко измельченный карбид кальция СаС2 при температуре около 1000 взаимодействует с азотом с образованием цианамида кальция CaCN2 по уравнению: CaC2 N2 CaCN2 C - - Q. В настоящее время роль этого метода в производстве связанного азота крайне незначительна. [13]
Сущность цианамидного метода заключается в том, что тонко измельченный карбид кальция СаС2 при температуре около 1000 взаимодействует с азотом с образованием цианамида кальция CaCN2 по уравнению: CaC2 N2 T CaCN2 C - f - Q. В настоящее время роль этого метода в производстве связанного азота крайне незначительна. [14]
Приготовленная смесь - карбидная шихта - загружается в цианамидную печь, через которую пропускают чистый азот. Образование цианамида кальция идет с большим выделением теплоты, которой достаточно для поддержания в печи нужной температуры, поэтому вскоре после начала реакции подогрев выключают. В результате пылевидный карбид кальция превращается в твердую, темную массу - цианамид кальция, коюрую переносят для охлаждения в специальное помещение. [15]
Страницы: 1 2