Образование - гидроксокомплекс
Cтраница 2
Растворимость осадка возрастает и в случае гидролиза катиона с образованием гидроксокомплексов. При учете такого влияния руководствуются аналогичными руссуждениями. [16]
Те металлы, электродные потенциалы которых в щелочной среде вследствие образования гидроксокомплексов понижаются и имеют более отрицательные значения, чем потенциал водорода, и те металлы, у которых оксидные и гидроксидные пленки на поверхности ( тормозящие взаимодействие металлов с водой) растворяются в щелочах. [17]
 |
Кривые титрования р. з. э. [18] |
Если же допустить, что пятый эквивалент щелочи расходуется на образование гидроксокомплекса LnY ( OH), то подобное же явление должно было бы наблюдаться и в комплексах ТМТУ вследствие аналогичной структуры. [19]
Растворение амфотерных гидроксидов в щелочных растворах обычно рассматривается как процесс образования гидроксокомплексов. [20]
Растворение амфотерных гидроксидов п щелочных растворах обычно рассматривают как процесс образования гидроксокомплексов. Широко применяемый в химической литературе алюминат-ион А102 - в растворе не существует. [21]
Электрохимические системы, используемые в серебряно-цинковых и никелево-кадмиевых щелочных аккумуляторах включают образование гидроксокомплексов цинка или кадмия. [22]
С увеличением рН возможность отрыва протона от ОН-группы возрастает и одновременно увеличивается вероятность образования гидроксокомплексов. Экспериментальные методы не позволяют различить эти два процесса. [23]
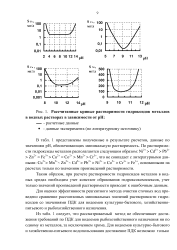 |
Рассчитанные кривые растворимости гидроксидов металлов в водных растворах в зависимости от рН. [24] |
Таким образом, при расчете растворимости гидроксидов металлов в водных средах необходим учет констант образования гидроксокомплексов, учет только значений произведений растворимости приводит к ошибочным данным. [25]
 |
Зависимость логарифма реальной константы устойчивости lg КГ2 от рН водного раствора в случае системы Ag - NH3. [26] |
Максимальное значение наблюдается при таких значениях рН, при которых как протонирование, так и образование гидроксокомплексов протекает в наименьшей степени. Левая ветвь кривой - нисходящая по той причине, что с увеличением кислотности раствора увеличивается степень протонирования. Правая ветвь - нисходящая потому, что с увеличением рН раствора увеличивается концентрация гидрок-сид-ионов, следовательно, усиливается образование гидроксокомплексов. [27]
При использовании более высоких концентраций органического реагента кривые экстракции сдвигаются в сторону больших кислотностей, и образование гидроксокомплексов, таким образом, затрудняется. [28]
 |
Зависимость диссо -, причем, как правило, чем выше циации ЭДТА от рН заряд иона, тем прочнее комплекс. [29] |
Помимо основной реакции комп-лексообразования в системе М - ЭДТА - Н2О протекают конкурентные реакции протонирования ЭДТА, образования гидроксокомплексов ме - S-i - JO / F lit талла ( см. разд. [30]
Страницы: 1 2 3 4