Образование - гомолог
Cтраница 3
Распадение амаровой кислоты на бензойную и пирамаровую и состав последней указывали на существование в амаровой кислоте эфиловой группы С2Н5; чтобы решить положительно вопрос о присутствии или отсутствии такой группы в амаровой кислоте, представляется два ближайших пути: или путь исследования различных производных из пирамаровой кислоты - путь, так сказать, аналитический, или образование гомологов амаровой и пирамаровой кислот с другими спиртными группами - путь синтетический; я избрал последний. Нужно было решить, в каком процессе соединяется спиртная группа: в процессе ли образования бензамарина, при действии воздуха и едкого кали на спиртный раствор дезоксибензоина или при разложении бензамарина кипящим спиртным раствором кали или натра. [31]
Поскольку процесс замещения, имеющий место в данном случае, аналогичен процессу алкилирования, при введении алкиль-ных групп в моноалкилбензолы можно ждать о -, - ориентации. При образовании трехзамещенных гомологов бензола замещение приводит к образованию 1, 2, 4 - и 1, 3, 5 - производных бензола. Условия же опыта способствуют перегруппировке 1, 2, 4-трициклопентилбензола в более устойчивый 1, 3, 5-изомер. [32]
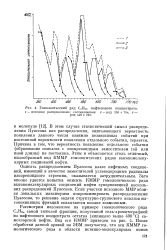 |
Гомологический ряд СПН2П нафтенового концентрата. [33] |
В этом случае статистический смысл распределения Пуассона как распределения, описывающего вероятность появления данного числа взаимно независимых событий при постоянной вероятности появления отдельного события, теряется. Причина в том, что вероятность появления отдельного события ( образование гомолога с изопреноидным заместителем той или иной длины) не постоянна. Этим и объясняется столь отличный пилообразный вид КММР гомологических рядов высокомолекулярных соединений нефти. [34]
Изомер значительно менее активен; пропокси - и бутоксианалоги джиплура совершенно неактивны. Применение в описанном выше синтезе лесквереловой кислоты вместо рицинолевой привело к образованию гомолога, правая часть которого имеет на две метиленовые группы больше, чем у джиплура. Это вещество оказалось значительно менее активным, чем джиплур. [35]
Однако последние данные свидетельствуют о том, что реальная причина избирательного действия ароксиалкилкарбоно-вых кислот имеет более сложный характер. Существуют растения, в которых наряду с р-окислением протекает еще более быстрый процесс образования высших алифатических гомологов - вероятно, путем присоединения малонового эфира. Таким образом, феноксимасляные кислоты выводятся из растений главным - образом в виде феноксиалкилкарбоновых кислот с длинной алифатической цепью. [36]
Продукты реакции проходят далее зону закалки водой, где быстро охлаждаются до 80 С, благодаря чему реакция разложения ацетилена замедляется. В процессе термоокислительного пиролиза метана, кроме основной реакции образования ацетилена, протекают побочные реакции образования гомологов ацетилена и других ненасыщенных углеводородов, сажи и смолы. Часть образующейся сажи осаждается и уплотняется на стенках реакционного канала. Реакционную и закалочную воду отделяют во влагоотделителе 6, а основную масс у газа через свечу 7 направляют для сжигания в факеле. [37]
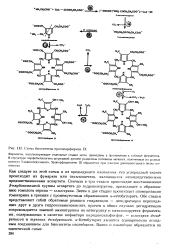 |
Схема биосинтеза протопорфирина IX. [38] |
Как следует из этой схемы и из предыдущего изложения, ого углеродный скелет происходит из фумарата или оксалоацетата, являющихся непосредственными предшественниками аспартата. Сначала в три стадии происходит восстановление - карбоксильной группы аспартата до гидроксигруппы, приводящее к образованию гомолога серина - гомосерииа. Затем в две стадии происходит изомеризация гомосерина в треонин с промежуточным образованием а-кетобутирата. Обе стадии представляют собой обратимые реакции гидратации - дегидратации переходящих друг в друга гидроксиаминокислот, причем в обоих случаях дегидратация сопровождается заменой аминогруппы на кетогруппу и катализируется ферментами, содержащими в качестве кофактора пиридоксальфос-фат, - юмосерин дегид-ратазой и треонин дегидратазой. Кетобутират является одновременно исходным соединением для биосинтеза изолейцнна. [39]
Во всех случаях значительную роль играет реакция дегидрогенизации с превращением тетралина в нафталин. При температуре 580 С около 50 % превращенного тетралина реагирует с разрывом тетраме-тиленовой цепочки и образованием гомологов бензола и около 40 % подвергается реакции дегидрогенизации с образованием нафталина. По мере повышения температуры ( и глубины) крекинга роль реакции дегидрогенизации быстро возрастает. [40]
По данным И. Б. Рапопорта [10] хинолин при температуре 210 - 220 и давлении 100 - 110 ати в присутствии MoS2 почти нацело превращается в гидрохинолин. Последний при 420 - 450 и 200 ати в присутствии этого же катализатора легко расщепляется с образованием гомологов пиридина и углеводородов. С повышением температуры количество оснований снижается, а количество углеводородов повышается. Образование ароматических углеводородов происходит путем отщепления группы NH2 и насыщения свободной связи углерода водородом. [41]
Процесс проводится при температурах 100 - 300 С, давлении 5 - 40 атм, молярном отношении водорода и углеводородов 1: 4, Расход водорода составляет 4 - 8 л на 1 л жидкого сырья. Катализатор не корродирует аппаратуру и не чувствителен к присутствию ароматических углеводородов, поскольку они подвергаются каталитическому гидрированию с образованием гомологов циклогексана, которые в свою очередь изоме-ризуются. Соединения серы отравляют гидрирующий компонент катализатора, вызывая необходимость предварительного обес-серивания исходного сырья. Если в сырье содержится более 1 10 - 2 % воды, то она блокирует активные центры, что затрудняет доступ к ним молекул углеводородов. [42]
Процесс проводится при температурах 1ОО - 300 С, давлении 5 - 40 атм, молярном отношении водорода и углеводородов 1: 4, Расход водорода составляет 4 - 8 л на 1 л жидкого сырья. Катализатор не корродирует аппаратуру и не чувствителен к присутствию ароматических углеводородов, поскольку они подвергаются каталитическому гидрированию с образованием гомологов циклогексана, которые в свою очередь изоме - ризуются. Соединения серы отравляют гидрирующий компонент катализатора, вызывая необходимость предварительного обес - серивания исходного сырья. Если в сырье содержится более 1 - 10 - 2 % воды, то она блокирует активные центры, что затрудняет доступ к ним молекул углеводородов. [43]
Известен ряд методов синтеза винилацетата на основе ацетилена, этилена и других исходных продуктов. Ацетилен не должен содержать реакционноспособных примесей ( метилацетилена, сернистых соединений и особенно соединений с двойными или тройными связями), которые могут приводить к образованию гомологов винилацетата. Допускаются лишь небольшие примеси азота, двуокиси углерода, водорода. [44]
Повторяя этот процесс нужное количество раз, можно притти к формуле желаемого гомолога. Преимущество этого определения Сеньор видит в том, что оно сразу дает схему для классификации типов гомологии, потому что в каждом частном случае описанный процесс образования гомолога определяет значение трех переменных, а именно: 1) число связей, разомкнутых во время всего процесса; 2) какая именно связь размыкалась на каждой единичной стадии; 3) структурный тип двухвалентного алкиленового радикала, включаемого после каждого последовательного размыкания. Однако прежде чем перейти к рассмотрению этих трех переменных, Сеньор вводит понятие так называемого эталонного соединения и рассматривает в дальнейшем лишь группы высших структурных гомологов этих конкретных, исходных, эталонных соединений. [45]
Страницы: 1 2 3 4