Образование - двуокись - углерод
Cтраница 1
Образование двуокиси углерода происходит за счет уменьшения содержания ценной окиси углерода; однако этого можно избежать подбором соответствующего катализатора. Образование метана также является отрицательным явлением; его нельзя окончательно устранить, но, тщательно выбрав условия проведения процесса, можно свести до минимума. [1]
Образование двуокиси углерода и изобутил-о-толуидина, СН3С6Н4 - NH - СН2 - СН ( СН3) 2, объясняется ш перегонкой а-о-толуидино-изовалериановой кислоты. [2]
Образование двуокиси углерода и формальдегида, по-видимому, является независимой реакцией, а не результатом дальнейших превращений глиоксалевой кислоты; на это указывает экстраполирование выходов продуктов реакции до нулевой дозы облучения с целью исключения неопределенности результатов. [3]
Теплота образования двуокиси углерода равна - 393 6 кдж. Сколько литров двуокиси углерода, измеренной при нормальных условиях, образовалось, если выделилось 209 3 кдж тепла. [4]
Теплоты образования двуокиси углерода и воды из элементов при 17 С равны соответственно ДЯсо, - 94 05 и ДЯн о - - 68 318 ккал. Теплота сгорания метана при этой же температуре равна - 211 93 ккал / моль. [5]
Скорость, образования двуокиси углерода с увеличением концентрации перекиси водорода вначале растет, однако начиная с некоторой концентрации она снижается. [6]
На скорость образования двуокиси углерода переход во второй температурный интервал ( 270 - 320 С) заметного влияния не оказывает. Количество этого продукта регулярно растет вплоть до 1 моля на моль октана при 400 С, после чего с дальнейшим повышением температуры остается практически неизменным. [7]
Зная теплоты образования двуокиси углерода ( 94 ккал), окиси углерода ( 26 4 ккал) и водяного пара 57 8 ккал), докажите, что процесс получения генератор ного газа должен сопровождаться выделением тепла, а процесс получения водяного газа - поглощением тепла. [8]
Реакция характеризуется образованием двуокиси углерода и осадка окиси железа. В большинстве случаев реакция сопровождается выделением тепла и часто протекает очень бурно. [9]
Реакция характеризуется образованием двуокиси углерода и осадка окиси железа. В большинстве случаев реакция сопровождается выделением тепла и часто протекает очень бурно. [10]
 |
Зависимость износа анодов от кислотности анолита. [11] |
Окисление графита с образованием двуокиси углерода и небольших количеств окиси углерода приводит также к нарушению связи между отдельными зернами графита и механическому осыпанию частиц анода. [12]
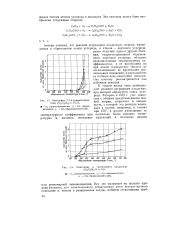 |
Окисление 2 2 4-триметилпен-тана ( 02 / С8Н1812 3. [13] |
Реакция, сопровождающаяся образованием двуокиси углерода, обладает незначительным температурным коэффициентом, в ее протекании ни при какой температуре ( вплоть до воспламенения) не происходит значительных изменений, и удельный вес ее в общем ходе окисления невелик. Она поэтому рассматривается как побочная реакция. [14]
Реакция эта весьма напоминает образование двуокиси углерода из карбоновой кислоты, озоциановой кислоты из мочевины, или же кетена из ацетона. [15]
Страницы: 1 2 3 4