Образование - двуокись - углерод
Cтраница 2
Перечислите известные вам источники образования двуокиси углерода в природе, быту и промышленности. [16]
Определение углерода ( по образованию двуокиси углерода) могло иметь значение разве лишь для установления, что данное вещество - органическое. Определение водорода ( по образованию воды при сжигании органических соединений, что было открыто еще Ван Гельмонтом) могло также представлять ограниченный интерес. [17]
С под давлением с образованием двуокиси углерода и продукта, в результате перегонки которого получается ацет-анилид. [18]
С проба сжигается с образованием двуокиси углерода, воды, газообразного галоидоводорода ИЛРГ двуокиси серы в зависимости от химического состава анализируемой пробы. [19]
Если вся ВПК используется для образования двуокиси углерода и воды, то требующееся количество кислорода будет равно конечному ВПК в сутки. В связи с тем, что часть ВПК не используется для окисления, необходимо внести поправку на количество образующихся клеток с учетом ежесуточных потерь. [20]
Для солей угольной кислоты характерно образование двуокиси углерода при действии на них кислот. Карбонаты разлагаются при более высокой температуре, чем гидрокарбонаты. [21]
Более глубокое окисление приводит к образованию двуокиси углерода и воды. [22]
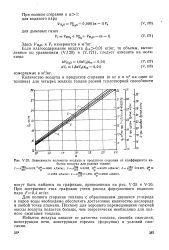 |
Зависимость количеств воздуха и продуктов сгорания от коэффициента избытка воздуха для разных топлив. [23] |
Для полного сгорания топлива с образованием двуокиси углерода и паров воды необходимо обеспечить достаточное количество кислорода в любой точке пламени. Поэтому для хорошего перемешивания горючей массы воздуха подается больше, чем теоретически необходимо для полного сжигания топлива. [24]
Глюкоза и гликоген окисляются с образованием двуокиси углерода и воды в результате ряда химических реакций, составляющих два различных цикла. [25]
Фосген медленно гидролизуется водой с образованием двуокиси углерода и хлористого водорода. [26]
Щавелевая кислота легко окисляется с образованием двуокиси углерода и воды. [27]
 |
Зависимость количеств воздуха и продуктов сгорания от коэффициента из. [28] |
Для полного сгорания топлива с образованием двуокиси углерода и паров воды необходимо обеспечить достаточное количество кислорода в любой точке пламени. Поэтому для хорошего перемешивания горючей массы воздуха подается больше, чем теоретически необходимо для полного сжигания топлива. [29]
К - При стандартных условиях теплоты образования двуокиси углерода, метана и воды соответственно равны 393 51; 74 85 и 241 84 кдж / моль. [30]
Страницы: 1 2 3 4