Количественное образование
Cтраница 1
Количественное образование хлороводо рода близко к теоретически возможному. Необходимо отметить образование значительных количеств оксида углерода ( II), оксида углерода ( IV), винилхлорида, ароматических углеводородов. [1]
Практически количественное образование 1 1-дифторпропана из 1 3-дибромпропана может быть объяснено двухстадийным фторированием через возникновение резонансно-стабилизированного фторированного катиона. [2]
Количественное образование оксида углерода зависит от условий горения, температуры и недостатка кислорода воздуха, а также вида горения. Так, при получении генераторного газа ( термоокислительное разложение древесины) до 48 5 % всего углерода древесины удается превратить в оксид углерода. Остальная часть углерода расходуется на образование простых и сложных веществ. [3]
В случае триметилсилилпроизводного количественное образование гексаметилдисилоксана при действии 5 % раствора NaOH происходит в течение одной минуты. Однако связь Si - С в этих сульфо-нах более устойчива к расщеплению кислотами, чем в соответствующих кремнеорганических кетонах, нитрилах и сложных эфирах. [4]
Он основан на количественном образовании альдринфенилдигид-ротриазола при нагревании альдрина с избытком фенилазина, удалении непрореагировавшего азида вакуумной отгонкой, обработки остатка триазола спиртовым раствором НС1 и избытком диазотированного 2 4-динитроанилина. Полученное красное ди-азосоединение определяют колориметрически или спектрометрически в сильно кислой среде. [5]
Подтверждением этого может служить количественное образование уксусной кислоты при использовании N-нитроазоацетанилида в качестве инициатора полимеризации метплметакрилата. [6]
Таким образом, для количественного образования гидразона достаточен 7 - 10-кратный избыток гидразина. [7]
Условия, необходимые для количественного образования комплексов молибдена и вольфрама, были предметом значительных исследований, и полученные данные свидетельствуют о существовании некоторых противоречий. Однако ясно, что комплекс молибдена образуется в кислой области рН, и что при этом не требуется восстановителей. В отношении вольфрама высказаны два совершенно различных предложения: согласно одному из них реакция проводится в горячей сильно кислой среде в присутствии восстановителя, согласно другому - реакция дол-лена идти в горячем слабокислом растворе без добавления восстановителя. [8]
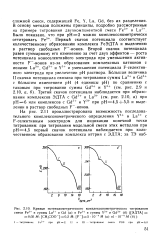 |
Кривые потенциометрического комплексонометрического титрования. [9] |
Первый скачок потенциала соответствует количественному образованию комплекса РеЭДТА и выделению в раствор свободных Р - - ионов. Второй скачок потенциала равен суммарному его изменению за счет двух эффектов - роста потенциала ионоселективйого электрода при уменьшении активности Р - - ионов из-за образования комплексных катионов с ионами La3, Gd3 и Y3 и уменьшения потенциала Р - селектив-ного электрода при увеличении рН раствора. Третий скачок потенциала наблюдается при образовании комплексов ЭДТА с Gd3 и La3 ( см. рис. 2.10, а) при рН 6 или комплексов с Gd3 и Y3 при pH4 5 - f - 5 5 и выделении в раствор свободных Р - - ионов. [10]
Подтверждением этой схемы служит также количественное образование ( CsHs TiCb при действии НС1 на раствор конечного продукта реакции f ( CsHsbTi ] в тетрагидрофуране. [11]
Обязательным условием получения правильных результатов является количественное образование фенилгидразона из исследуемого карбонильного соединения. Это осуществимо далеко не для всех карбонильных соединений. В описанных ниже условиях ( нагревание в течение 15 мин при 100 С) удалось провести реакцию приблизительно на 100 % со всеми истинными альдегидами. Кетоны, у которых карбонильная группа находится в гидроароматическом кольце или между двумя бензольными кольцами, в этих условиях количественно не реагируют ( за исключением флуорено на); углеводы также количественно не реагируют. Другие соединения, например а-дикетоны ( бензил, бензоилацетон) и хиноны реагируют менее чем с одним молем фенилгидразина или вообще не реагируют. Точность метода не очень велика, но вполне достаточна для того, чтобы, имея малое количество вещества неизвестного строения, установить, сколько реакционноспособных карбонильных групп содержится в его молекуле. [12]
В том случае, когда происходит количественное образование более стабильных изомеров, имеет место проявление вторичной реакции, которая также влияет на состав конечного продукта восстановления. Эта реакция заключается в эпимеризации алкоголят-ных комплексов. [13]
Чтобы сдвинуть это равновесие в направлении количественного образования серной кислоты, необходимо добавить вещество, связывающее серную и иодистоводородную кислоты. Таким веществом является пиридин. Кроме того, пиридин образует с сернистым ангидридом продукт присоединения и таким образом затрудняет улетучивание сернистого ангидрида из раствора. [14]
Это соединение присоединяет йодистый метил с количественным образованием четвертичного аммониевого соединения, которое растворимо в воде и совершенно неожиданно очень устойчиво. Оно разлагается лишь после кипячения в воде в течение 5 час. [15]
Страницы: 1 2 3 4