Кинетическое кривое образование
Cтраница 1
Кинетические кривые образования и накопления продуктов окисления изопропилового спирта молекулярным кислородом в жидкой фазе ( / 115 С, р 30 атм): 1 - переписные соединения ( суммарно перекись водорода и органические оксигидропере-кисные соединения); 2 - ацетон. [1]
 |
Зависимость потери в 85. Зависимость количества образовав. [2] |
Кинетические кривые образования этих газов, приведенные на рис. 85, обнаруживают период индукции. [3]
Кинетические кривые образования полимера, изомеров с внутренней двойной связью и ЭЦГ, а также кривые общей убыли мономера в ходе полимеризации на каталитических системах, указанных в табл. 1.12, приведены на рис. 5.3 и 5.4. На основании этих кривых сделан вывод, что основным процессом при взаимодействии ВЦГ с комплексными металлоор-ганическими катализаторами является его полимеризация. Скорость полимеризации на всех применяемых каталитических системах максимальна в начальный период, а затем постепенно уменьшается. Превращение ВЦГ в изомеры с внутренней двойной связью и ЭЦГ протекает значительно медленнее и уже через 20 - 40 мин после начала полимеризации практически прекращается. Только в случае системы А1 ( изо - С4Н9) 3 TiCl4 скорость изомеризации через 3 4 ч еще значительна и превышает скорость полимеризации ВЦГ примерно в 2 - 2 5 раза. [4]
 |
Подпрограмма гидропере. [5] |
Кинетические кривые образования перекисей и других продуктов аналогичны кривым, полученным при окислении пропана. Они имеют линейные участки и области насыщения. При повышении температуры is продуктах окисления, наряду с перекисью, появляются: при окислении метана - формальдегид, при окислении пропана - ацетальдешд и формальдегид. Начиная с 200, выход перекиси, метила и этила с дальнейшим повышением температуры начинает падать, между тем ьак гыход альдегидов непрерывно растет. [6]
 |
Спектры низкомолекулярных продуктов окисления пентапласта ( растворы в СС14.| Накопление летучих продуктов окисления пентапласта при 140 С. [7] |
Кинетические кривые образования воды, окиси и двуокиси углерода и водорода ( рис. 60) показывают, что уже за 2 ч окисления при 140 С процесс проходит очень глубоко. К этому времени 49 % поглощенного кислорода приходится на долю воды, окиси и двуокиси углерода. [8]
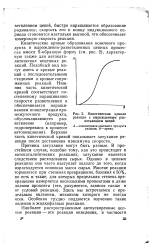 |
Кинетическая кривая реакции с вырожденным разветвлением цепей. [9] |
Кинетические кривые образования конечного продукта в вырожденно-разветвленных цепных процессах имеют S-образную форму ( см. рис. 2), характерную также для автокаталитических нецепных реакций. Подобный вид могут иметь и кривые реакций с последовательными стадиями и кривые сопряженных реакций. [10]
Анализ кинетических кривых образования летучих веществ - суммарных продуктов распада - и карбоидов - продуктов уплотнения - показал, что при повышенном давлении повышение температуры от 40 до 470 С приводит к увеличению продуктов распада не более чем в 3 раза, тогда как количество продуктов уплотнения может увеличиться более чем в 20 раз. [11]
Во-вторых, кинетические кривые образования кислот при различных условиях ведения непрерывного процесса окисления парафина показывают, что скорость окисления изменяется во времени, в начальный период высокая и затем низкая. Можно предположить, что скорость реакции определяется истинной скоростью реакции с участием катализатора. Очевидно, активным катализатором являются соединения, марганца высших валентностей. Это подтверждается зависимостью между скоростью окисления и изменением относительного содержания марганца высшей валентности. [12]
На рис. 32 представлены кинетические кривые образования бисфенолов при кислотжжаталитических реакциях формальдегида с ди - грет - бути л фенол а ми к различных растворителях. Ип приведенных данных следует, что в реакциях с формальдегидом в условиях кислотного катализа 2 4-диалкил фенолы обладают значительной реакционной способностью и с высоким выходом образуют соответствующие бисфснолы, а 2 6-диалкилфснолы в эту реакцию практически не вступают. [14]
 |
Продукты окисления углеводородов в присутствии озона. [15] |
Страницы: 1 2 3
